CATS 임상결과 위약∙니코틴대체제 대비
챔픽스의 심혈관계 이상반응 유의한 차이 없는 것으로 나타나
심혈관질환 환자 대상 EVITA 임상 통해
높은 금연치료 효과 및 안전성 확인
올해 세계 금연의 날 주제 ‘흡연과 심장질환’,
심혈관질환 환자들의 금연치료 현황도 발표
한국화이자제약(대표이사 사장 오동욱, www.pfizer.co.kr)이 ‘세계 금연의 날’을 맞아 5월 30일 기자간담회를 열고, 자사의 챔픽스(성분명: 바레니클린타르타르산염)가 대규모 글로벌 임상연구 CATS와 EVITA를 통해 금연치료 보조요법으로서의 효과와 심혈관계 안전성을 재확인했다고 발표했다.
CATS 임상결과 위약∙니코틴대체제 대비 챔픽스의 심혈관계 이상반응에 유의한 차이가 없는 것으로 나타남에 따라1, 챔픽스는 지난 2016년 발표된 EAGLES 연구 를 통한 신경정신과적 안전성 확인에 이어 심혈관계 안전성에 대한 근거도 확보하게 됐다.
CATS(Study To Evaluate Cardiac Assessments Following Different Treatments Of Smoking Cessation Medications In Subjects With And Without Psychiatric Disorders)는 전세계 최대 규모의 금연치료 글로벌 임상인 EAGLES (Evaluating Adverse Events in a Global Smoking Cessation Study)의 연장 연구로, EAGLES에 참여했던 8,058명의 성인 흡연자 가운데 4,595명을 대상으로 기존 연구의 12주 치료 및 12주 관찰 이후 추가적인 28주의 추적 관찰을 통해, 챔픽스, 부프로피온, 니코틴대체제 및 위약의 심혈관계 이상반응 관련 안전성을 비교한 연구다.1 이는 지난 4월 10일 JAMA(Journal of the American Medical Association)지에 게재된 바 있다.
이 연구의 1차 평가변수(primary endpoint)는 금연치료 중 주요 심혈관계 이상반응이 일어나기까지 걸리는 시간이었고, 2차 평가변수(secondary endpoint)는 모든 주요 심혈관계 이상반응 발생과 함께 말초동맥질환 발병, 울혈성 심부전, 불안정형 협심증, 심각한 부정맥 등으로 설정됐다.1 총 52주에 걸쳐 진행된 연구에서 흡연자는 매 4주마다 모든 이상반응, 혈압, 심박수, 니코틴 사용 및 일산화탄소 배출 정도를 검사 받았다.1 연구 결과 챔픽스 투여군과 부프로피온, 니코틴대체제, 위약 투여군의 심혈관계 이상반응, 혈압, 심박수 변화 등에 유의미한 차이가 나타나지 않는 것으로 확인됐으며, 주요 심혈관계 이상반응 발생 시간에서도 유의미한 차이가 발견되지 않았다.1
이어서 발표된 EVITA(Evaluation of Varenicline (Champix) in Smoking Cessation for Patients Post-Acute Coronary Syndrome)는 심혈관질환 환자인 흡연자를 대상으로 챔픽스의 효과와 심혈관계 이상반응과 관련한 안전성을 확인한 연구다.2 미국과 캐나다에서 심근경색 등 급성관상동맥증후군으로 입원한 302명의 흡연자들을 대상으로 각 환자들이 퇴원 전 금연치료를 시작해 12주 간 챔픽스군과 위약군으로 대조하는 방식으로 진행됐으며, 총 24주의 후속 관찰(follow-up)을 통해 금연 여부 및 일산화탄소 수치 검사를 시행했다.2
연구의 1차 평가변수는 24주차의 금연율이었으며, 2차 평가변수는 지속적인 금연, 부작용 및 중대한 이상반응 관련 안전성 평가 등으로 구성됐다.2 그 결과 24주차의 금연율은 챔픽스군 47.3%, 위약군 32.5%로 확인됐으며 이상반응으로 인한 치료 중단은 챔픽스군 11.3%, 위약군 12.8%로 나타났다.2 주요 심혈관계 이상반응은 챔픽스군 4.0%, 위약군 4.6%로 나타나 심혈관 관련 이상반응에서도 챔픽스의 안전성을 확인했다.2 해당 연구는 미국심장협회(American Heart Association) 학술지에 2015년 11월에 게재된 바 있다.
EVITA 연구의 책임 연구자였던 아이젠버그 박사는 “글로벌 대규모 임상연구 CATS와 EVITA의 연구결과는 심혈관계 질환을 동반한 흡연자들의 금연치료에 있어서 심혈관계 이상반응에 대한 의학적 근거를 제공한다는 점에서 큰 의미가 있다”고 강조하였다.
아이젠버그 박사는 “심혈관질환 환자들은 반드시 금연을 통해 심각한 심혈관계 위험성을 감소시켜야 하는 만큼, 의지만으로 금연이 어려울 경우 임상을 통해 효과와 안전성이 확인된 금연치료가 옵션이 될 수 있다”고 설명했다.
분당서울대병원 가정의학과 이기헌 교수는 올해 WHO가 ‘세계 금연의 날’의 주제로 선정한 ‘흡연과 심장질환’에 초점을 맞춰, 흡연량과 심혈관질환 발생의 상관관계에 대해 발표하고 다양한 관련 임상결과들을 소개했다.
특히 흡연이 심혈관질환의 발생 위험 증가에 미치는 영향과 금연을 통한 위험 감소 효과에 대해 설명하면서, 이 교수는 “담배는 조금만 피우더라도 심혈관질환의 발병 위험이 급격히 증가하기 때문에 흡연량을 줄이는 것만으로는 심장마비나 사망의 위험을 낮출 수 없다”며 “만성질환을 가진 중증흡연자들은 금연이 어려울 경우 효과와 안전성이 확인된 금연치료를 통해 반드시 금연을 해야 심혈관질환 위험을 줄일 수 있다”고 강조했다.
한국화이자제약 의학부 총괄 강성식 상무는 “금연치료 보조요법의 심혈관계 안전성에 대한 의학적 근거들을 바탕으로, 심혈관질환 환자들과 의료진들이 보다 안심하고 금연치료를 활용할 수 있을 것으로 기대한다”며, “한국화이자제약은 앞으로도 ‘담배 없는 세상’, ‘니코틴 없는 세상’을 위해 금연치료에 신뢰를 줄 수 있는 다양한 연구에 최선을 다할 것”이라고 말했다.
CATS 연구1
CATS 연구는 16개국에서 화이자와 글락소스미스클라인(GSK)이 함께 진행한 무작위, 평행군, 이중맹검, 위약 및 니코틴 대체요법 대조 임상연구인 EAGLES 연구3의 비치료 연장 임상시험이다. 본 연구는 EAGLES 연구에서 진행한 12주의 챔픽스, 부프로피온, 니코틴 패치, 위약 활용 금연치료와 12주 관찰기간 이후 추가적인 28주의 추적 관찰을 통해 금연치료의 심혈관계(CV) 안전성 데이터를 구축했다.
연구의 한계: 해당 연구결과는 급성 혹은 불안정한 심혈관질환을 가진 환자들을 분석 대상에 포함하지 않았던 점에서 한계가 있지만, 일반적인 흡연자들의 챔픽스 복용은 심혈관계 이상반응을 유의미하게 증가시키지 않는다는 점은 확인됐다.
연구의 1차 평가변수(primary endpoint)는 금연치료 중 심혈관질환에 의한 사망, 비치명적 심근경색, 비치명적 뇌졸중 등의 주요 심혈관계 이상반응(MACE: Major Adverse Cardiovascular Events)이 일어나기까지 걸리는 시간이었으며, 2차 평가변수(secondary endpoint)는 모든 주요 심혈관계 이상반응의 발생과 함께 말초동맥질환이 새롭게 발병하거나 질환이 악화되어 시술이 필요한 경우, 울혈성 심부전으로 인한 입원, 관상동맥혈관재생술, 또는 불안정형 협심증, 심각한 부정맥으로 입원하는 경우, 비치명적인 심근경색과 뇌졸중의 발생, 심혈관질환에 의한 사망 등(MACE+)으로 설정됐다.
총 52주까지 진행된 연구에서 총 4,595명의 흡연자는 매 4주마다 시험 클리닉을 방문해 모든 이상반응, 혈압, 심박수, 자기 보고 니코틴 사용 및 일산화탄소 배출 정도를 검사 받았으며, 심혈관질환 이상반응은 2명의 심장 전문의, 신경과 전문의로 구성된 독립된 위원회에 의해 검토와 판결이 이뤄졌다. 연구 결과 챔픽스 투여군과 부프로피온, 니코틴대체제, 위약 투여군의 심혈관계 이상반응, 혈압, 심박수 변화 등에 유의미한 차이가 나타나지 않는 것이 확인됐으며, 주요 심혈관계 이상반응 발생 시간에서도 유의미한 차이가 발견되지 않았다.
안전성 평가변수에서 주요 심혈관계 사건(MACE)에 대한 챔픽스–위약의 위험도 차이(RDs, Risk Differences)는 −0.99(95% CI −4.80 ~ 2.82)였으며 부프로피온-위약의 위험도 차이(RDs)는 −0.08(95% CI −2.63 ~ 2.48), 챔픽스-부프로피온의 위험도 차이(RDs)는 −0.91(95% CI −4.78 ~ 2.96), 챔픽스-니코틴 패치 위험도 차이(RDs)는 −0.69(95% CI −4.63 ~ 3.26)로 나타났다. 말초동맥질환의 발병 등의 기타 주요한 심혈관질환 발생(MACE+)에서도 챔픽스–위약의 위험도 차이(RDs)는 −0.48(95% CI −2.75 ~ 1.80)이었으며 부프로피온-위약의 위험도 차이(RDs)는 0.11(95% CI −2.04 ~ 2.25), 챔픽스-부프로피온의 위험도 차이(RDs)는 −0.59(95% CI −2.84 ~ 1.67), 챔픽스-니코틴 패치 위험도 차이(RDs)는 −0.32(95% CI −2.65 ~ 2.01)로 나타났다.
EVITA 연구2
EVITA는 미국과 캐나다에서 심근경색 등의 급성관상동맥증후군으로 입원한 302명의 흡연자들을 대상으로 금연치료의 효과와 심혈관계 이상반응 관련 안전성을 살펴본 임상 연구로, 연구 대상 심혈관질환 환자는 퇴원 전 금연치료를 시작해 12주 간 챔픽스군과 위약 대조군으로 나뉘어 진행되었으며, 총 24주의 후속 관찰(follow-up)을 통해 금연여부 및 일산화탄소 수치 검사가 이뤄졌다.
연구의 1차 평가변수(primary endpoint)는 24주차의 금연율이었으며 2차 평가변수(secondary endpoint)는 지속적인 금연, 부작용 및 중대한 이상반응 관련 안전성 평가 등으로 구성됐다. 임상 과정 중 흡연율은 점진적으로 감소했다. 연구결과 4주, 12주, 24주에 챔픽스군으로 무작위 배정된 환자가 위약군 대비 흡연 금욕 및 감소율이 유의하게 높았다. 24주차의 금연율은 챔픽스군 47.3%, 위약군 32.5%로 확인됐으며, 흡연 횟수가 50% 이상 감소한 경우는 24주차에 챔픽스군 67.4%, 위약군 55.6%로 유의미한 차이가 확인됐다.
임상참여자 전반에서 가장 흔히 나타난 이상반응은 불면증(챔픽스군 17.9%, 위약군 12.6%), 오심(챔픽스군 13.9%, 위약군 8.6%), 비정상적인 꿈(챔픽스군 15.2%, 위약군 4.6%)으로 나타났으며 이상반응으로 인한 치료 중단은 챔픽스군 11.3%, 위약군 12.8%로 확인됐다. 주요 심혈관계 이상반응(MACE)은 챔픽스군 4.0%, 위약군 4.6%로 나타났다.
EAGLES 연구3
EAGLES 연구는 16개국에서 화이자가 글락소스미스클라인(GSK)과 함께 진행한 무작위, 평행군, 이중맹검, 위약 및 니코틴 대체요법 대조 임상연구다. 본 연구는 12주 이상의 기간 동안 금연치료 목적으로 챔픽스, 부프로피온, 니코틴 패치 혹은 위약을 사용하는 환자들에서 우울, 불안, 자살 관념 및 행동과 같은 중등증 및 중증의 신경정신과적 이상반응의 발생률을 알아보기 위해 미 식품의약국(FDA) 및 유럽의약국(EMA)의 요청을 받고 진행됐으며 연구의 설계 또한 기관들과의 협의를 통해 진행됐다.
연구의 한계: 해당 연구결과는 신경정신과적 질환을 가지고 있으나 치료받고 있지 않거나 안정적이지 않은 상태의 흡연자들에 대해서 일반화될 수 없다. 더불어 이번 연구에는 희귀한 신경정신과적 이상반응은 포함되지 않았을 수 있다.
EAGLES 연구의 1차 안전성 평가변수는 금연치료로 인해 발생한 불안, 우울, 비정상적 감정 혹은 적대감과 같은 신경정신과적 중증 이상반응 중 최소 한 가지와 초조, 공격, 망상, 환각, 살인 충동, 조증, 공황, 편집증, 자살 충동, 자살 시도 등 중증의 이상 반응 중 최소 한 가지의 발생이었다. 정신질환 병력이 없는 환자들에서 나타난 1차 안전성 평가변수의 발생률은 각각 챔픽스군 1.3%, 부프로피온군 2.2%, 니코틴 대체제군 2.5%, 위약군 2.4%였다. 정신질환 병력이 있는 환자들에서 1차 평가변수 발생률은 챔픽스군 6.5%, 부프로피온군 6.7%, 니코틴 대체제군 5.2%, 위약군4.9%로 나타났다.
정신질환 병력이 없는 환자들의 경우, 1차 안전성 평가변수에 대한 챔픽스–위약의 위험도 차이(RDs, Risk Differences)는 −1.28(95% CI −2.40 ~ −0.15)였으며, 부프로피온–위약의 위험도 차이(RDs)는 −0.08(−1.37 ~ 1.21)이었다. 챔픽스-니코틴 패치의 위험도 차이(RDs) 및 부프로피온-니코틴 패치의 위험도 차이(RDs)는 각각 −1.07(−2.21 ~ 0.08) 및 0.13(−1.19 ~ 1.45)이었다. 정신질환 병력이 있는 환자들인 경우, 챔픽스–위약의 위험도 차이(RDs) 및 부프로피온–위약의 위험도 차이(RDs)가 1.59(−0.42 ~ 3.59) 및 1.78(−0.24 ~ 3.81)이었고, 이에 비해 챔픽스-니코틴 대체제의 위험도 차이(RDs) 및 부프로피온-니코틴 패치의 위험도 차이(RDs)는 각각 1.22(−0.81 ~ 3.25) 및 1.42(−0.63 ~ 3.46)였다. 챔픽스와 부프로피온 치료군 모두 이러한 위험도 차이와 관련된 95%의 신뢰구간은 0 이하였다. 위약군을 포함해 모든 치료군에서 정신질환 병력이 있는 환자군에서 신경정신과적 이상반응이 더 많이 나타났다. 임상 참여자 전반에서 가장 흔히 나타난 이상반응은 오심(25.3%, 챔픽스군), 불면증(12.2%, 부프로피온군), 비정상적인 꿈(12.4%, 니코틴 패치군), 두통(9.9%, 위약군)이었다.
한국화이자제약
한국화이자제약은 글로벌 제약업계를 선도하는 화이자 그룹의 한국법인이다. 면역&염증, 심혈관&대사, 암, 백신, 신경과학&통증, 바이오시밀러&희귀질환 등 주요 핵심 R&D 분야와 관련된 혁신적인 치료제 및 다양한 포트폴리오 제품을 제공하고 있다. 한국화이자는 최고의 제품과 차별화된 서비스, 업계를 선도하는 프로그램을 통해 고객 만족을 실현하고 있으며, 국민 건강 증진과 국내 의약업계 발전에 기여하고 있다. 글로벌 임상시험유치∙ R&D 전문가 양성∙ 기술력 및 정보 공유∙ 전략적 제휴 노력 등 다각적인 활동을 펼쳐 국내 R&D 및 보건의료산업 발전에 끊임없이 기여하고 있다. 또한 책임 있는 기업 시민으로서 더불어 건강한 세상을 만들기 위해 ‘조손가정 행복만들기 캠페인’, ‘화이자 의학상’, ‘헬시에이징(Healthy Aging) 캠페인 등 다양한 사회공헌 활동을 지속적으로 펼치고 있다. www.pfizer.co.kr
챔픽스 (성분명: 바레니클린)
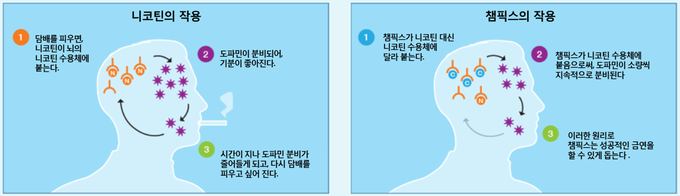
챔픽스는 뇌의 니코틴 수용체에 니코틴 대신 부분적으로 결합해 직접적으로 니코틴 중독을 해결해줌으로써 금단증상과 금연 욕구를 줄이는 데 도움을 준다.
챔픽스(바레니클린)는 의료진의 진단과 처방이 필요한 전문의약품으로, 여러 건의 임상연구 결과 12주 기준 금연성공률이 40~50%대%로 니코틴 대체제 및 부프로피온 등 다른 금연치료 옵션 대비 높은 금연치료 보조 효과를 확인했다.
특히, 한국인 및 대만인을 대상으로 한 임상연구에서는 12주 금연성공률이 약 60% 로 위약 대비 더 높게 나타난 바 있다. 상담요법과 함께 12주 치료의 80% 이상 챔픽스를 복용한 경우 6개월 후 금연 성공률은 52.2%로 나타났으며, 80% 미만을 복용하면 금연 성공률은 25.4%로 2배 이상 떨어진다 . 챔픽스는 금연치료의 보조요법으로 지난 2007년 3월 한국 식품의약품안전처의 허가를 받은 바 있다 .
References
1 Benowitz, N. L., Pipe, A., West, R., Hays, J. T., Tonstad, S., McRae, T., ... & Anthenelli, R. M. (2018). Cardiovascular Safety of Varenicline, Bupropion, and Nicotine Patch in Smokers: A Randomized Clinical Trial. JAMA internal medicine.
2 Eisenberg, M. J., Windle, S. B., Roy, N., Old, W., Grondin, F. R., Bata, I., ... & Cassavar, D. (2016). Varenicline for Smoking Cessation in Hospitalized Patients With Acute Coronary SyndromeCLINICAL PERSPECTIVE. Circulation, 133(1), 21-30.
3 Anthenelli, R. M., Benowitz, N. L., West, R., St Aubin, L., McRae, T., Lawrence, D., ... & Evins, A. E. (2016). Neuropsychiatric safety and efficacy of varenicline, bupropion, and nicotine patch in smokers with and without psychiatric disorders (EAGLES): a double-blind, randomised, placebo-controlled clinical trial. The Lancet, 387(10037), 2507-2520.
4 Efficacy and Safety of Varenicline for Smoking Cessation, The American Journal of Medicine (2008) Vol 121
5 Gonzales D, et al. Varenicline, α4β2 Nicotonic Acetylcholine receptor partial agonist, vs. sustained-release Bupropion and placebo for smoking cessation: a randomized controlled trial (JAMA July 5, 2006, Vol 296, No 1)
6 Aubin H-J et al. Varenicline versus transdermal nicotine patch for smoking cessation; results from a randomized open-label trial (Thorax, 2008;63:717-724)
7 Douglas E, et al. Efficacy of Varenicline, an α4β2 Nicotonic Acetylcholine receptor partial agonist, vs. placebo or sustained-release Bupropion for smoking cessation (JAMA July 5, 2006, Vol 296, No. 1)
8 Nides M, et al. Varenicline versus bupropion SR or placebo for smoking cessation: a pooled analysis (Am J Health Behav 2008 Nov-Dec;32(6):664-75)
9 Tsai S, et al. A randomized, placebo-controlled trial of Varenicline, a selective α4β2 Nicotonic Acetylcholine receptor partial agonist, as a new therapy for smoking cessation in Asian smokers (Clinical Therapeutics 2007 Vol. 29, #6)
10 Catz SL, Jack LM, McClure JB, et al. Adherence to varenicline in the COMPASS smoking cessation intervention trial. Nicotine Tob Res. 2011;13(5):361-8.