세계 최초 FDA 승인 받은 불활화 4가 인플루엔자(독감) 백신
‘플루아릭스 테트라’는 세계 최초로 FDA 승인을 받은4-9 불활화 4가 인플루엔자 백신이다. 미국•한국뿐 아니라 영국•독일•호주 등 전 세계 35개국 허가기관의 기준을 통과했다. 전 세계적으로 약 1억 도즈 이상 공급10돼 사용 경험을 축적해 왔으며, 미국, 영국, 호주의 국가예방접종사업(NIP) 백신에 선정되어 사용되고 있다.
한편, ‘플루아릭스 테트라’가 생산되는 독일 드레스덴2 생산 설비는 세계적인 기준에 부합하는 백신을 생산하기 위해 GSK품질관리조직의 내부 감사는 물론 미국 FDA, 유럽의약품청, 그리고 각 허가당국의 정기적인 감사를 받고 있다. 독일 생산 설비에서 1도즈의 ‘플루아릭스 테트라’가 생산되기까지 약 350회의 품질 검사가 이루어진다.16
국내 최초 •국내 1위1 4가 인플루엔자 백신
‘플루아릭스 테트라’는 국내에서 최초로 승인된 4가 인플루엔자 백신으로21 2016년 국내에 소개된 4가 인플루엔자 백신 중 판매 1위를 달성하였다.1 2015년 이후 국내에서 출시한 신약의 판매액 집계 결과, ‘플루아릭스 테트라’는 백신부문 1위, 전체 전문의약품 중 판매 4위를 기록 **, 가장 성공적인 백신 신제품으로 평가 받고 있다.
또한, 최근 실시된 연구에 따르면 국내에서 ‘플루아릭스 테트라’를 접종한 환자는 다른 백신을 접종한 환자그룹보다 동일한 백신으로 재접종 하겠다는 응답자가 많았다. ***
당뇨병∙고혈압∙심혈관질환 등 모든 만성질환 환자 접종 가능
‘플루아릭스 테트라’는 면역체계가 취약한 65세 이상 고령자에서 높은 항체방어율(SPR)과 항체전환율(SCR)을 보여 미국 FDA와 유럽 EMA 허가기준을 충족, 고령자에서도 면역원성을 입증했다. 또한 인플루엔자 고위험군인 당뇨병, 만성호흡기질환, 심뇌혈관질환, 만성간질환, 암 등 만성질환자를 포함한 임상 연구에서 면역원성과 안전성 데이터를 확인, 만성질환자가 접종 가능한 4가 인플루엔자 백신이다.26
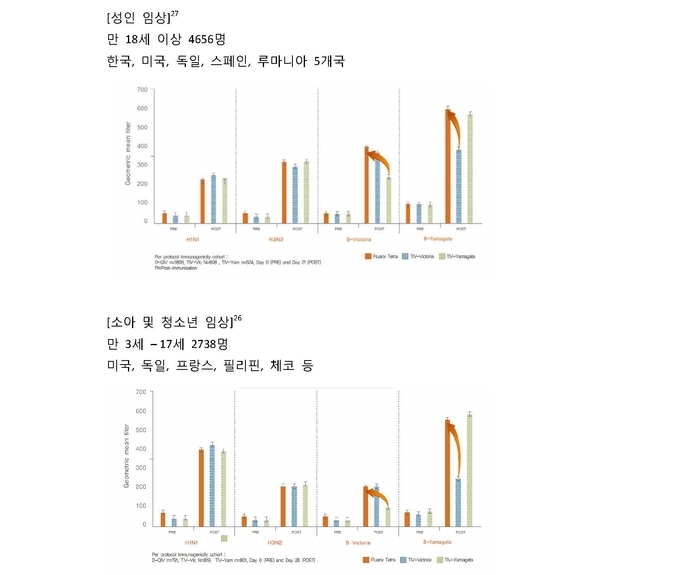
[‘플루아릭스 테트라’ 의 대규모 글로벌 임상 결과]26
‘플루아릭스 테트라’는 면역원성과 안전성 데이터를 확인하기 위해 소아 및 청소년, 성인 대상으로 실시한 대규모 글로벌 임상 연구 결과, 3가 백신 대비 추가된 B형 바이러스에 대해 우월한 면역원성을 보였다. 공통되는 세가지 인플루엔자 균주에 대해서는 3가 백신과 비교하여 유사한 면역원성을 입증했고, 국소, 전신 이상반응에서 3가 백신과 유사한 안전성 프로파일을 보였다.
|
의약품 명[i]
|
플루아릭스 테트라 프리필드시린지
(인플루엔자 분할백신)
|
|
효능·효과2
|
- 만 3세 이상의 소아 및 성인에서 이 백신에 포함된 인플루엔자 A형 바이러스들 및 인플루엔자 B형 바이러스들에 의해 유발되는 인플루엔자(독감) 질환의 예방
|
|
용법·용량2
|
- 만 3세 이상의 소아 및 성인에서 1회 0.5ml를 근육 주사하고, 같은 용량으로 매년 1회 접종한다. 단, 이전에 인플루엔자 백신을 접종하지 않은 9세 미만의 소아의 경우에는 4주 이상의 간격을 두고 2회 접종한다.
|
|
국내 승인·출시일
|
- 식품의약품안전청 승인: 2014년
12월 26일[ii]
- 국내 출시: 2015년
04월
|
전 세계 백신 판매량 1위 GSK
세계적인 백신명가 GSK는 매일 약 200만 도즈의 백신을 생산하여 160여 개국에 공급하는 판매량 1위 기업이다. GSK는 국내에서도 15종 이상의 백신을 출시하여 소아, 성인의 질병 예방을 위해 노력하고 있다.
*인용데이터: 2016년 2Q~2017년 1Q IMS Sales Audit 참조. IMS 데이터는 패널로부터 받은 유통자료를 통계 처리한 추정치로써 실제와 다를 수 있으며, IMS는 본 데이터의 활용으로부터 발생하는 분쟁에 대하여 여타의 책임을 지지 않음.
**인용데이터: 2016년 Q4 MAT IMS Sales Audit 참조. IMS 데이터는 패널로부터 받은 유통자료를 통계 처리한 추정치로써 실제와 다를 수 있으며, IMS는 본 데이터의 활용으로부터 발생하는 분쟁에 대하여 여타의 책임을 지지 않음.
*** 연구시기인 2015-16년 인플루엔자 시즌에는 플루아릭스 테트라가 4가 인플루엔자 백신으로 한국에서 단독으로 유통되었다.
References
1 IMS data, Influenza Vaccine sales, 2017 1Q
5 US FDA, December 14, 2012 approval letter • Fluarix Quadrivalent
6 US FDA, June 7, 2013 Approval Letter - Fluzone Quadrivalent
7 US FDA, August 15, 2013 Approval Letter - FluLaval Quadravalent
8 US FDA, May 23, 2016 Approval Letter - Flucelvax Quadrivalent
9 US FDA, August 26, 2016 Approval Letter -AFLURIA QUADRIVALENT
10 GSK Data on file(전세계허가국 현황 및 공급현황)
14 The National Flu Immunisation Programme 2016/17 by NHS England
15 Australian government department of health, Immunise
16 GSK data on file (GSK Biologicals Dresden your manufacturer for Fluarix Tetra)
22 IMS Sales Audit Q4 MAT
23 Hyeongap Jang, GSK Vaccine R&D,Factors affecting influenza vaccination in 50-64 years old elderly_170224
24 식약처 플루아릭스테트라 품목허가증 (2014.12.26)
25 B. Weinberger, Vaccines for the elderly, European Society of Clinical Microbiology and Infectious Diseases, CMI, 18 (Suppl. 5), 100–108
26 Kieninger D et al. BMC Infect Dis 2013;13:343
27 Domachowske JB, et al. A randomized trial of candidate inactivated quadrivalent influenza vaccine versus trivalent influenza vaccines in children aged 3-17 years. J Infect Dis. 2013; 207: 1878-1887.
28 IMS 2016 1Q Vaccine volume 기준
30 GSK data on file(OPAL_Registrations)