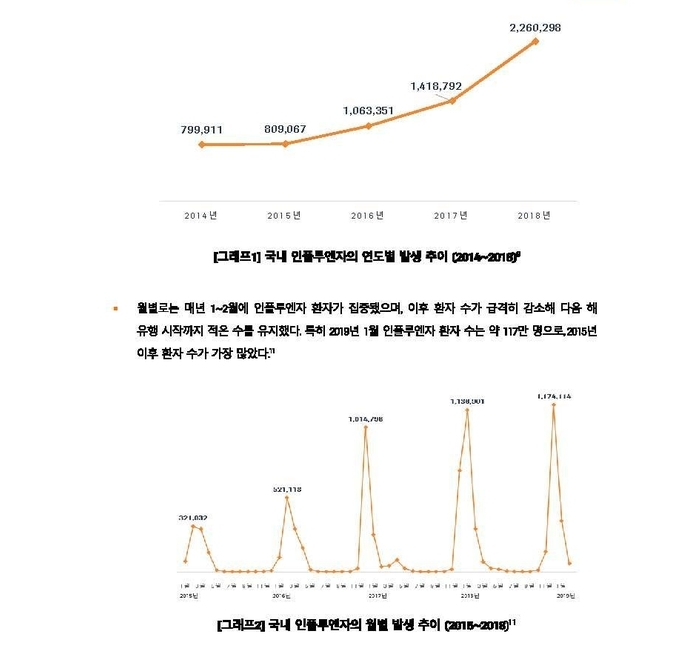
2018년 국내 인플루엔자 환자 약 200만 명, 연간 사망자는 700명 이상 추정
전 세계에서 인플루엔자로 인해 연간 약 13조 원의 의료비 지출 및 약 1,500만 일의 근무일 손실 등 사회 경제적 부담 야기
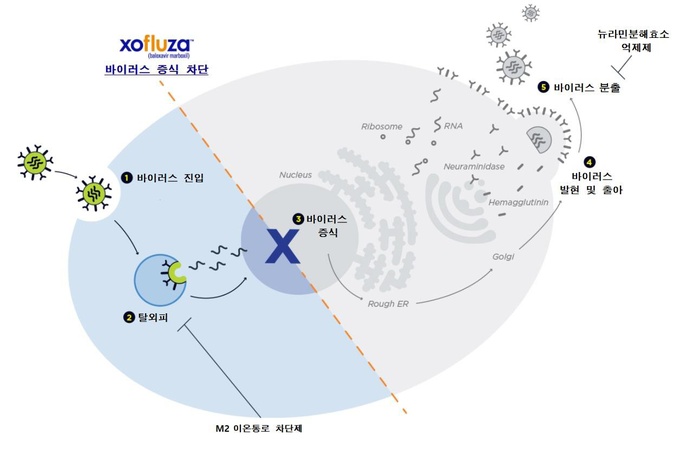
약 20년 만에 개발된 새로운 기전 가진 조플루자, 단 1회 경구 복용으로 신속한 증상 완화 및 전염 예방에 도움 줄 것으로 기대
㈜한국로슈(대표이사 닉 호리지)는 12월 17일 서울 웨스틴조선 호텔에서 자사 인플루엔자 치료제 조플루자(성분명 발록사비르마르복실)의 국내 허가를 맞아 인플루엔자 치료 패러다임 전환을 주제로 「조플루자 허가 기자 간담회」를 개최했다.
조플루자는 단 한 번 경구 복용으로 인플루엔자 증상을 신속하게 완화시킬 뿐 아니라, 인플루엔자 바이러스가 검출되는 시간을 단축시켜 전염 예방에도 도움이 될 수 있는 치료 옵션이다.
이번 기자 간담회는 고려대학교 감염내과 정희진 교수의 인플루엔자 국내·외 통계와 심각성 및 그로 인해 야기되는 사회적 문제 등에 대한 발표를 시작으로, 한림대학교 감염내과 이재갑 교수의 인플루엔자 치료 현황 및 조플루자 주요 임상 데이터에 대한 소개로 이어졌다.
인플루엔자는 단순히 심한 감기가 아니라 경우에 따라서는 사망까지 이를 수 있는 치명적인 감염성 질환이다. 매년 전 세계에서 약 10억 명이 계절성 인플루엔자에 감염되며 이 중 약 25~50만 명의 사망자가 발생하는 것으로 알려져 있다.
국내에서도 2018년을 기준으로 약 200만 명이 인플루엔자로 진단 받았으며, 연간 700명 이상이 인플루엔자로 인해 사망하는 것으로 추정된다. 특히 전체 인구의 25~35%가 인플루엔자에 감염되는 ‘인플루엔자 대유행(pandemic influenza)’이 발생했을 시 전 세계 사망자 수가 약 7,100만 명까지 급증하기도 한다.
이번 기자 간담회에 자리한 애론 허트(Dr. Aeron Hurt) 로슈 글로벌 인플루엔자 의학부 디렉터는 “인플루엔자는 가족 중 한 명이 감염되면 다른 가족에게 전염될 확률이 38%에 달할 정도로 전염력이 강할 뿐 아니라, 이로 인해 연간 약 13조 300억 원(약 1,120억 달러)의 추가적인 의료비 지출이 야기된다(미국 기준)”며, “인플루엔자로 인해 매년 약 1,500만 일의 근무일 손실이 발생하고 있어 (미국 기준) 사회적 부담 또한 큰 것으로 알려져 있다”고 설명했다.
그러나 현재 인플루엔자 치료에는 항바이러스제 내성으로 인해 단 한 가지 계열(뉴라미니다아제)의 약제만 권고되고 있을 뿐 아니라, 기존 경구용 인플루엔자 치료제는 5일 동안 복용해야 하므로 복약 순응도 측면에서 한계가 있다. 또한 인플루엔자는 전염 속도가 빠르기 때문에 인플루엔자 바이러스가 검출되는 시간을 단축시켜 전염 예방에 도움이 될 수 있는 치료 옵션의 필요성이 높았다.
최근 국내 허가를 획득한 조플루자는 약 20년 만에 개발된 새로운 작용 기전의 항바이러스제로, 인플루엔자 바이러스의 복제에 필수적인 중합효소 산성 엔도뉴클레아제(polymerase acidic endonuclease)를 억제해 바이러스의 복제 초기 단계부터 진행을 막고, 바이러스 증식을 미연에 방지한다.
특히 조플루자는 임상연구에서 단 한 번의 경구 복용으로 합병증을 동반하지 않은 환자(12세 이상, 64세 이하)군과 고위험군 환자군(12세 이상) 모두의 증상을 신속하게 완화시킬 뿐 아니라 인플루엔자 바이러스가 검출되는 환자들의 비율을 빠르게 감소시켜 향후 인플루엔자 전염 예방에도 도움이 될 수 있을 것으로 기대된다. 또한 합병증을 동반하지 않은 환자(12세 이상, 64세 이하)를 대상으로 진행된 연구에서 전체 이상반응(AE, Adverse Event) 발생률은 조플루자 투여군(20.7%)에서 위약(24.6%)과 오셀타미비르 투여군(24.8%) 대비 가장 낮았다.
한림대학교 감염내과 이재갑 교수는 발표를 통해 “조플루자는 단 1회 경구 복용을 통해, 5일 동안 복용해야 하는 기존 경구 인플루엔자 치료제의 한계로 지적됐던 복약 순응도를 개선할 수 있을 것”이라며 “이를 통해 조플루자가 인플루엔자 환자들의 증상을 신속하게 완화할 뿐 아니라, 장기적으로는 국내 인플루엔자 관리에도 긍정적인 영향을 줄 것으로 기대하고 있다”고 전했다.
한편 조플루자는 지난 11월 22일 성인 및 만 12세 이상 청소년의 인플루엔자 A형 또는 B형 바이러스 감염증의 치료로 식품의약품안전처 허가를 획득했다. 현재 조플루자는 일본, 미국, 대만, 홍콩 등 한국을 포함해 총 12개 국가에서 허가를 받아 사용되고 있다.
CAPSTONE-1 임상연구에 대하여5
CAPSTONE-1은 미국과 일본의 합병증을 동반하지 않은 12세 이상 인플루엔자 환자 총 1,436명을 대상으로 조플루자의 유효성과 안전성을 연구한 다기관, 무작위, 이중맹검 3상 대조군 임상연구다.
연구에 참여한 환자들은 조플루자 투여군(40mg 또는80mg, 1회 복용), 오셀타미비르 투여군(75mg, 1일 2회, 총 5일간 투여), 위약투 여군(matching with treatment group)으로 무작위 배정됐다.1차 평가변수는 증상 완화까지 소요 시간이며, 주요 결과는 다음과 같다.5
• 조플루자 투여군은 53.7시간(95% CI: 49.5-58.5 시간)의 인플루엔자 증상 완화까지 소요 시간 중간값을 나타내, 위약 투여군(80.2시간, 95% CI: 72.6-87.1시간) 대비 환자들의 증상 지속시간을 약 26.5시간 단축시킴(P<0.001)5
• 조플루자 투여군은 해열까지 24.5시간의 소요 시간 중간값을 나타내, 위약 투여군(42.0시간) 대비 해열까지 소요되는 시간을 약 17.5시간 단축시킴(P<0.001)5
• 각 투여군에서 바이러스 검출 중단까지의 소요 시간 중간값은 조플루자 투여군에서 24.0시간, 오셀타미비르 투여군에서 72.0시간, 위약군에서 96.0시간으로, 조플루자Ⓡ 투여군에서 가장 짧았음(P<0.001)5
• 전체 투여군중 조플루자 투여군의 전체 이상반응 발현 비율은 20.7%로, 위약(24.6%) 및 오셀타미비르 투여군(24.8%) 대비 낮은 수치를 보임5. 가장 흔한 이상반응은 설사(3.0%), 기관지염(2.6%), 메스꺼움(1.3%), 부비동염(1.1%)이었으며, 해당 이상반응은 위약 투여군 대비 낮은 빈도로 발생했음
CAPSTONE-2 임상연구에 대하여6
CAPSTONE-2는 12세 이상 인플루엔자 합병증 고위험군 환자를 대상으로 오셀타미비르 및 위약 대비 조플루자의 유효성과 안전성을 연구한 다기관, 무작위, 이중맹검 3상 임상연구다.
미국 질병관리본부(CDC, The Centers for Disease Control and Prevention)는 인플루엔자 환자중 천식, 만성폐질환, 당뇨, 심장질환, 고도비만과 같은 만성질환을 동반한 환자, 그리고 65세 이상의 고령 환자들을 인플루엔자 합병증 고위험군으로 규정하고 있다. 해당 글로벌 임상연구는 일본 시오노기사가 수행했다.
임상연구에 참여한 환자들은 조플루자 투여군(40mg 또는 80mg, 1회복용), 오셀타미비르 투여군(75mg, 1일 2회, 총 5일간 투여), 위약군(1일 2회, 총 5일간 투여)으로 무작위 배정됐다. 1차 평가변수는 증상완화까지 소요시간이었으며, 주요 결과는 다음과 같다.
• 인플루엔자 고위험군 환자들을 대상으로 조플루자 투여군은 약 73시간의 증상완화까지 소요시간 중간값을 나타내, 위약 투여군(약 102시간) 대비 약 29시간 단축된 결과를 보임 (P<0.001)
• 특히 조플루자는 B형 인플루엔자 바이러스 환자들의 증상완화까지 소요시간 중간값(약 75시간)을 위약(약 101시간) 대비 약 26시간 단축시킴
• 임상연구를 통해 조플루자 치료를 받은 청소년, 그리고 성인 환자들에게서 보고된 이상반응은 설사(3%), 기관지염(3%), 구역(2%), 부비동염(2%), 두통(1%) 등이었음. 또한 조플루자의 내약성은 양호했으며, 새로운 안전성 징후(safety signal)는 발견되지 않음
References
1 건강보험심사평가원, 보건의료빅데이터개방시스템, 국민관심질병통계>>인플루엔자 (심사년도기준, 2014~2018)
2 통계청, 2018 사망원인통계
3 Carrat F, et al. Timelines of infection and disease in human influenza: a review of volunteer challenge studies. American Journal ofEpidemiology. 2008;167(7):775-785.
4 식품의약품안전처, 의약품안전나라(의약품통합정보시스템), 조플루자정40밀리그램(발록사비르마르복실)
5 Hayden FG, et al. Baloxavir Marboxil for Uncomplicated Influenza in Adults and Adolescents. N Engl J Med 2018; 379:913-923
6 Ison MG et al. Phase 3 Trial of Baloxavir Marboxil in High-Risk Influenza Patients (CAPSTONE-2 Study) Open Forum Infect Dis 2018;5(suppl1):S764
7 질병관리본부, 2019-2020절기인플루엔자관리지침
8 질병관리본부, 인플루엔자대유행대비•대응계획(교육자료) (accessed in November 2019)
9 World Bank. Evaluating the Economic Consequences of Avian Influenza. Possible economic consequences of a human pandemic (page 3). [Intranet; cited 2019 July]
10 Tsang, T. K., et al. Household transmission of influenza virus. Trends Microbiol. 2016 Feb.; 24(2):123-133
11 Putri WCWS, et al. Economic burden of seasonal influenza in the United States. Vaccine, 20128 June 22;36(27):3960-3966
12 Keech M, et al. The impact of influenza and influenza-like illness on productivity and healthcare resource utilization in a working population. Occup Med 1998;48(2): 85-90
13 Uyeki T.M., et al. Clinical Practice Guidelines by the Infectious Diseases Society of America: 2018 Update on Diagnosis, Treatment, Chemoprophylaxis, and Institutional Outbreak Management of Seasonal Influenza
15 질병관리본부감염병포털, 표본감시감염병통계정보(인플루엔자), 2018~2019년