● 유전성 혈관부종, 환자마다
부종의 빈도와 중증도, 증상 발생부위가 다양한 희귀질환으로 증상 예측조차 어려워 응급 상황 발생 시
신속한 대처 요구돼
● 유전성 혈관부종 급성 부종(acute attacks) 증상 치료제 피라지르®, 기존 2회분에서 최대 4회분까지
처방 가능하도록 급여기준 확대돼 환자들의 치료 접근성 개선
● 예측할 수 없는 급성 부종 증상으로 인해 신체적 위축과
심리적 불안[i] 속에서 살아가는 환자들의 미충족 수요를 해소하는 데 중요한 의미를 가지는 진전
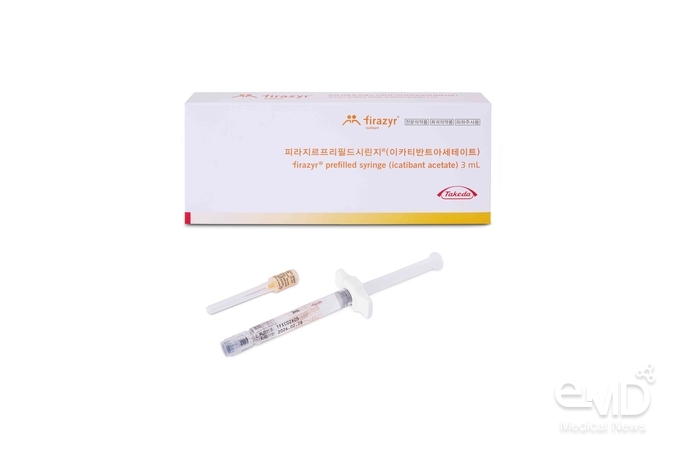
한국다케다제약은 자사의 유전성 혈관부종(HAE) 급성 부종(acute attacks) 증상 치료제 ‘피라지르®프리필드시린지(Firazyr®, 성분명: 이카티반트아세테이트, 이하 피라지르®)’의 건강보험 급여 적용범위가 12월 1일부터 처방 당 최대 4회분으로 확대 적용됐다고 밝혔다.
피라지르®는 2014년 6월 국내 허가 이후,[2] 2018년 9월 성인 환자를 대상으로 1회분 급여가 적용됐으며,[3]
이어 2019년 7월에는 만 2세 이상의 소아까지 사용 연령을 확대해 다양한 연령대에서 응급상황에 신속히 대처할 수 있는 기반을 마련했다.[4]
2021년 3월부터는 처방당 2회분까지 급여가 시행되며[5] 추가적인 급성 부종 증상에 대비할 수 있는 환경이 조성됐다.
이번 급여 확대는 발생 시점과 중증도를 예측하기 어려운 급성 부종의 특성상,[6] 처방당 최대 2회분 급여 인정의 한계와 국내 HAE 환자들의 치료 접근성 강화를 위한 필요성이 반영된 결과다. HAE 환자들은 첫 급성 부종 증상 발생 시 잔여 보유 중인 치료제 부족에 대한 우려로 인해 초기 증상에도 약물 사용을 주저하는 상황이 반복됐다.[7]
이는 국제 치료 지침의 '급성 부종 증상 발생 초기에 신속히 치료해야 한다'는 권고사항과 상충되며,[8]
환자 및 의료진은 유전성 혈관부종 질환 관리의 적시성과 안전성 측면에서 개선이 필요하다는 목소리를 지속 제기했다.
이에 보건복지부와 건강보험심사평가원은 교과서, 임상진료지침, 전문가 의견 등을 종합적으로 검토해 잦은 급성 부종 증상을 경험했거나 추가 투여가 필요했던 환자를 대상으로 피라지르®의 급여를 처방당 4회분까지 확대하기로 결정했다.2 이는 기존 처방당 최대 2회분 급여 시행 이후 약 3년 9개월 만에 이뤄진 조치로, 국내 유전성 혈관부종 환자들을 위한 안정적인 치료 환경을 제공하고, 미충족 의료 수요를 해소하기 위한 한국다케다제약의 지속적인 노력이 담긴 결과로 평가된다.
한국다케다제약 희귀질환 사업부 김나경 총괄은 “이번 피라지르® 급여 확대는 국내 유전성 혈관부종 환자들에게 치료 접근성을 한층 강화하며, 국제 치료 가이드라인의 ‘급성 부종 증상 발생 초기에 신속히 치료해야 한다’는 권고사항을 실현한 중요한 진전”이라고 밝혔다. 이어 “급성 부종 증상으로 인해 불안과 위험 속에서 살아가는 환자들에게 더 안정적인 치료 환경을 제공할 수 있게 돼 기쁘게 생각한다”며, “한국다케다제약은 앞으로도 환자들이 생명을 위협할 수 있는 급성 부종으로부터 보다 나은 환경에서 치료받을 수 있도록 지원하며, 의료 사각지대에서의 어려움을 해소하기 위해 최선을 다할 것”이라고 덧붙였다.
유전성 혈관부종은 체내 ‘C1-에스테라제 억제제’ 결핍 혹은 기능 이상으로 인해 두드러기나 가려움증 없이 반복적으로 혈관부종을 유발하는 희귀질환이다.[9] 특히, 급성 부종이 상부 호흡기나 소화기관에 발생할 경우 기도폐색과 장폐색으로 이어질 수 있어10 신속하고 적절한 대응이 필수적이다. 급성 부종은 수 시간 내에 발생해 최대 5일까지도 증상이 지속될 수 있으며, 부종의 중증도를 가늠할 수 없다.7
피라지르는 C1-에스테라제 억제제 결핍으로 인한 만2세 이상 유전성 혈관부종의 급성 부종(acute attacks) 증상에 사용되는 응급 치료제로,3 브래디키닌(Bradykinin)의 혈관 확장 작용을 차단해 2시간 내 급성 부종을 완화한다.[10]
프리필드시린지(사전 충전형 주사기) 형태로 제공되기 때문에 의료 전문가의 적절한 지도를 받은 환자는 응급 상황에서도 스스로 피하 주사를 투여할 수 있어 신속한 대처가 가능하다.3
[2] 식품의약품안전처, 의약품안전나라 의약품통합정보시스템, 의약품상세정보, 피라지르, Available at: https://nedrug.mfds.go.kr/pbp/CCBBB01/getItemDetailCache?cacheSeq=201402853aupdateTs2024-11-18%2010:50:08.0b, Accessed in December 2024
[4] 식품의약품안전처, 의약품안전나라 의약품통합정보시스템, 의약품상세정보, 피라지르 용법용량 변경이력, Available at: https://nedrug.mfds.go.kr/pbp/CCBBB01/getItemChangeHistInfo?itemSeq=201402853&changeIemCode=107, Accessed in December 2024
[6] Bernstein, J. A. (2018). Severity of hereditary
angioedema, prevalence, and diagnostic considerations. Am J Manag
Care, 24(14 Suppl), S292-S298.
[7] 삶을 위협하는
희귀질환의 치료환경 개선을 위한 정책적 지원 모색, 김미애 국회의원, Available at: https://ampos.nanet.go.kr:7443/materialSeminarDetail.do?control_no=PAMP10000000076483, Accessed in December 2024
[8] Busse et al, US HAEA Medical Advisory Board 2020 Guidelines for the
Management of Hereditary Angioedema, J Allergy Clin Immunol Pract.2021Jan;9(1):132-150
[9] 질병관리청. 희귀질환헬프라인. 희귀질환정보. D84.1 C1 에스터레이스억제인자결핍 Available at: https://helpline.kdca.go.kr/cdchelp/ph/rdiz/selectRdizInfDetail.do?menu=A0100&rdizCd=RA201810653, Accessed in December 2024
[10] Cicardi, M., Banerji, A.,
Bracho, F., Malbrán, A., Rosenkranz, B., Riedl, M., ... & Fan, W. T.
(2010). Icatibant, a new bradykinin-receptor antagonist, in hereditary
angioedema. New England Journal of Medicine, 363(6), 532-541.
[i] Chong-Neto, H. J. (2023). A
narrative review of recent literature of the quality of life in hereditary
angioedema patients. World Allergy Organization Journal, 16(3), 100758.