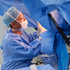
아일리아 프리필드시린지, 기존 바이알 제형서 허가받은 전체 적응증에 동일하게 보험 적용1
효과성, 안전성, 유연성 3박자 갖춘 아일리아® 6,7,8,9,10,11,12, 프리필드시린지 출시로 치료과정 ‘편의성’ 더해
아일리아®, T&E 요법 통해 최소 4주부터 최장 16주까지 현재 출시된 Anti-VEGF 가운데 가장 유연한 투여간격으로 환자 맞춤형 치료 선도3,4,5
바이엘 코리아(대표이사 프레다 린, 이하 '바이엘')는 습성 연령관련 황반변성(Wet Age-related Macular Degeneration, 이하wAMD)치료제 아일리아®의 프리필드시린지(Pre-filled Syringe) 제형을 10월 1일 국내 출시한다고 밝혔다.
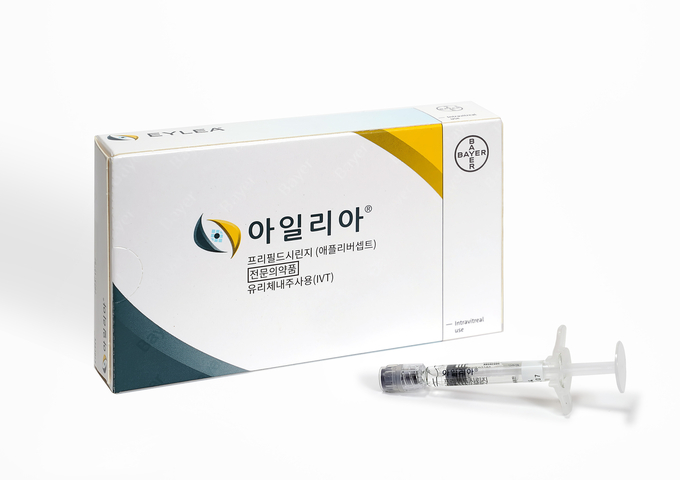
아일리아®프리필드시린지는 기존 아일리아® 바이알 제형에서 허가받은 전체 적응증(하단 [표1], [표2] 참고)에 사용할 수 있도록 허가됐으며 보험 역시 동일하게 적용된다.1 아일리아®는 프리필드시린지 제형 출시로 약물 투여 준비 시간을 줄여 환자와 의료진에게 보다 효율적이고 편리한 치료가 가능해졌다.
아일리아®프리필드시린지는 1mL 유리 시린지로 외관(Barrel)과 누름대(Plunger button)의 사이즈가 크며, 용량 기준선(dosage line) 확인도 용이하여 주사가 편리하다. 또한 주사기와 니들(needle)의 분리를 막는 장치인 루어락 어댑터(Luer-lock adaptor) 부분이 투명해 니들의 부착 상태 확인이 가능하고, 루어락 제거 방법은 돌려 따는(Twist off) 형식이다.
아일리아®는 2018년 wAMD 치료 시 첫 3개월 간 매달 주사 후 환자 상태에 따라 2주 또는 4주씩 투여 간격을 점진적으로 연장하여 최장 16주(4개월) 간격으로 투여 가능한 T&E 요법을 허가 받았다. 또한, 2022년 1월부터는 집중치료가 필요한 환자들을 위한 4주 간격 투여요법에 대한 급여가 가능해지면서 최소 4주에서 최장 16주까지 환자의 상태에 따라 투여간격을 가장 유연하게 조절할 수 있는3, 치료제로 자리매김하고 환자 맞춤형 치료를 선도하고 있다.
바이엘 코리아 의학부 문성철 총괄은 “아일리아®는 지난 10년간 전세계 환자 대상으로 진행된 각 적응증별 임상시험뿐만 아니라 실제 처방환경에서도 유효성과 안전성 프로파일을 입증해 왔으며, T&E 요법을 통해 현재 출시된 Anti-VEGF제품 중 가장 유연하게 투여간격을 조절할 수 있다. 치료의 ‘효과성’과 ‘안전성’ 그리고 투여간격의 ‘유연성’까지 3박자를 갖춘,,,,,, 아일리아®가 프리필드시린지 제형의 출시로 ‘편의성’을 더하며 환자와 의료진에게도 보다 나은 치료 환경을 제공할 수 있게 되어 기쁘다”고 전했다.
바이엘 코리아 특수의약품 사업부 서상옥 총괄은 “아일리아 프리필드시린지를 먼저 도입한 유럽국가에서는 프리필드시린지 제형 출시 이후 아일리아® 매출이 더 빠르게 성장했다.13,14 국내에서도 프리필드시린지 출시는 치열해지는 Anti-VEGF 시장에서 아일리아®가 No.1 황반변성 치료제18로서 입지를 더욱 굳건하는 계기가 될 것”이라고 밝혔다.
한편, 아일리아®는 2022년 5월 현재, 전세계적으로 5,400만개 이상이 판매되었고, 이를 바탕으로 연간 8백 만 명 이상의 처방경험(환자-년)이 축적됐다. 또한 국내에서는 2013년 출시 이후, 습성 연령관련 황반변성 치료, 망막정맥폐쇄성 황반부종에 의한 시력손상의 치료, 당뇨병성 황반부종에 의한 시력손상의 치료, 병적 근시로 인한 맥락막 신생혈관 형성에 따른 시력 손상의 치료에 사용되고 있으며, 5년동안 3,169명의 환자를 대상으로 실시한 시판 후 사용성적조사 결과에서도 임상시험과 일관된 안전성 프로파일을 보였다.
바이엘에 대하여

바이엘은 생명 과학 영역인 헬스케어와 농업 분야에서 핵심 역량을 지닌 글로벌 기업이다. 바이엘의 제품과 서비스는 세계 인구의 증가와 고령화에 따른 현 시대 주요 과제들에 대한 해결책을 찾는 데 기여함으로써 인류의 삶의 질을 개선하고자 한다. 바이엘은 지속 가능한 성장의 원칙 하에 혁신과 성장을 통한 수익의 극대화 및 가치 창출을 목표로 하며, 바이엘 브랜드는 전 세계적으로 믿음, 신뢰, 그리고 우수성을 상징한다. 2020년 회계연도 기준, 약 100,000 명의 임직원이 근무하고 있으며, 매출은 414억 유로, 그리고 R&D 투자는 49 억 유로에 달한다. 보다 자세한 정보는 www.bayer.com 에서 확인할 수 있다
References
1 건강보험심사평가원, PFS 결과통보문서
2 Introducing the new EYLEA pre-filled Syringe, PP- EYL-CA-0439-1
3 아일리아 국내 제품 설명서(개정년월일 2021.12)
4 대한안과학회공문, 바이엘코리아(주), 아일리아주사 8주미만 치료와 관련 허가 사항 변경 및 요양급여 인정의 건, 2022년 1월 26일
5 Lanzetta P, Loewenstein A, Vision Academy Steering Committee. Fundamental principles of an anti-VEGF treatment regimen: optimalapplication of intravitreal anti-vascular endothelial growth factor therapy of macular diseases. Graefes Arch Clin ExpOphthalmol. 2017;255(7):1259-12736.
6 Jeffrey S. Heier et al, Intravitreal Aflibercept (VEGF Trap-Eye) in Wet Age-related Macular Degeneration, Ophthalmology 2012;119:2537–2548
7 Kaiser PK, et al. Long-term safety and visual outcome of intravitreal aflibercept in neovascular age-related macular degeneration. Ophthalmology Retina 2017;1:304-313
8 David M. Brown, Intravitreal Aflibercept for Diabetic Macular Edema, Ophthalmology 2015; 122(10):2044-2052
9 Korobelnik JF, Do DV, Schmidt-Erfurth U, et al. Intravitreal aflibercept for diabetic macular edema. Ophthalmology 2014. 121(11):2247-54
10 Jeffrey S. Heier, MD, Intravitreal Aflibercept for Diabetic Macular Edema. Ophthalmology 2016; 123(11):2376-2385
11 Ogura Y, et al. Intravitreal Aflibercept for Macular Edema Secondary to Central Retinal Vein Occlusion 18-Month Results of the Phase 3 GALILEO Study, Am J Ophthalmol 2014; 158(5): 1032-1038
12 Yasushi Ikuno, Intravitreal Aflibercept Injection in Patients with Myopic Choroidal Neovascularization, Ophthalmology 2015; 122(6): 1220-1227
15 Data on file. 바이엘 보도자료 2020.2.10 배포(Bayer announces Phase III trials with new aflibercept 8mg formulation)
16 Ryu G. et al. Real-World Outcomes of Intravitreal Aflibercept for Neovascular Age-Related Macular Degeneration: A Large-Scale Postmarketing Surveillance in Korea. Clin Ophthalmol. 2021;15:3601-361
17. 보건복지부 고시 제2022-111호, 요양급여의 적용기준 및 방법에 관한 세부사항(약제) 일부개정고시
18. Data on file. Eylea (val&vol) Aug-18-2022

 바이엘은 생명 과학 영역인 헬스케어와 농업 분야에서 핵심 역량을 지닌 글로벌 기업이다. 바이엘의 제품과 서비스는 세계 인구의 증가와 고령화에 따른 현 시대 주요 과제들에 대한 해결책을 찾는 데 기여함으로써 인류의 삶의 질을 개선하고자 한다. 바이엘은 지속 가능한 성장의 원칙 하에 혁신과 성장을 통한 수익의 극대화 및 가치 창출을 목표로 하며, 바이엘 브랜드는 전 세계적으로 믿음, 신뢰, 그리고 우수성을 상징한다. 2020년 회계연도 기준, 약 100,000 명의 임직원이 근무하고 있으며, 매출은 414억 유로, 그리고 R&D 투자는 49 억 유로에 달한다. 보다 자세한 정보는 www.bayer.com 에서 확인할 수 있다
바이엘은 생명 과학 영역인 헬스케어와 농업 분야에서 핵심 역량을 지닌 글로벌 기업이다. 바이엘의 제품과 서비스는 세계 인구의 증가와 고령화에 따른 현 시대 주요 과제들에 대한 해결책을 찾는 데 기여함으로써 인류의 삶의 질을 개선하고자 한다. 바이엘은 지속 가능한 성장의 원칙 하에 혁신과 성장을 통한 수익의 극대화 및 가치 창출을 목표로 하며, 바이엘 브랜드는 전 세계적으로 믿음, 신뢰, 그리고 우수성을 상징한다. 2020년 회계연도 기준, 약 100,000 명의 임직원이 근무하고 있으며, 매출은 414억 유로, 그리고 R&D 투자는 49 억 유로에 달한다. 보다 자세한 정보는 www.bayer.com 에서 확인할 수 있다