“MSD ‘키트루다®’, 비소세포폐암 첫 치료부터
강력한 표준 치료 혜택 현실화
글로벌 표준 치료 키트루다, 급여 확대로 국내 새 표준 치료로 자리 잡을 것으로 기대
더 많은 국내 비소세포폐암∙호지킨림프종 환자, 최선의 치료 옵션 통한 생존 연장 기회 누릴 것
한국MSD(대표 케빈 피터스)는 3월 16일 오후 2시, 자사의 항 PD-1 면역항암제 ‘키트루다’(성분명: 펨브롤리주맙)의 비소세포폐암 1차 고식적 요법 및 호지킨림프종 건강보험 급여 확대1를 기념하는 “키트루다, 함께 내일을 이루다” 기자간담회를 열고, 급여 확대 의미와 키트루다의 차별적 치료 혜택에 대해 공유하는 자리를 가졌다.
국내 허가 면역항암제 중 최초로 폐암 1차 고식적 요법 치료 급여 확대1
모든 전이성∙진행성(Stage IV) 폐암 환자, 시작부터 최선의 치료 옵션 사용으로 두 배 더 많은 내일 기대
이 날 간담회에서 연세암병원 종양내과 폐암센터 홍민희 교수는 ‘키트루다의 비소세포폐암 1차 치료 임상적 가치와 혜택’을 주제로, 장기 생존 데이터로 살펴보는 키트루다의 임상적 유용성을 소개했다.
국내 암 사망률 1위인 폐암은 글로벌 가이드라인이 표준 치료로 권고하는 면역항암제 1차 치료를 통해 생존율 개선이 입증 되었음에도 불구하고 국내 폐암 환자 중 세포 독성 항암제 1차 치료 후 실패한 환자만 2차 이상 치료로 급여가 적용돼 오랜 기간 환자와 임상 현장의 간극이 있다고 지적되어 왔다.
이번 키트루다 폐암 1차 급여 확대로 전이성 비소세포폐암으로 진단된 편평/비편평상피세포암 포함 모든 환자가 1차 치료부터 데이터로 입증된 강력한 글로벌 표준 치료 혜택을 받을 수 있게 됐다.1
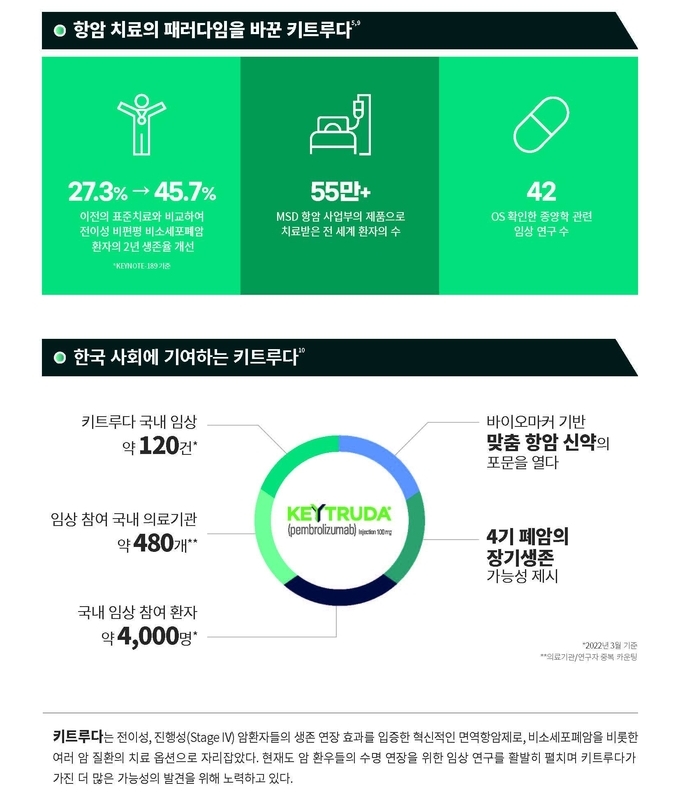
키트루다 1차 치료는 장기 생존 데이터를 통해 한결같이 강력한 치료 효과(OS, ORR)및 장기 생존율을 보여 주고 있으며 이미 글로벌 3상 임상 연구 및 FDA 허가 후 다년간의 치료 경험을 통해 임상적 유용성이 입증된 치료법이다. 다수의 연구 결과를 바탕으로 NCCN 등 글로벌 가이드라인에서는 키트루다 1차 치료를 전이성 비소세포폐암 1차 표준 치료로, 가장 높게 권고하고 있다.3
이번 급여 확대의 바탕이 된 전이성·진행성(Stage IV) 비소세포폐암 연구는 KEYNOTE-189, KEYNOTE-407, KEYNOTE-024 연구로 키트루다 1차 치료를 받은 환자는 기존에 표준 치료로 사용되던 항암화학요법 대비 약 2배 더 긴 생존기간을 보였고, 높은 반응률 및 삶의 질 개선을 보인 것으로 보고돼 급여 확대를 통해 보다 많은 비소세포폐암 환자들이 키트루다 1차 치료 혜택을 확인할 수 있게 됐다.4,5,6,
홍민희 교수는 “이번 폐암 1차 급여 확대는 많은 환자와 의료진이 오랫동안 기다려온 희망적인 소식으로, 국내 모든 전이성·진행성(Stage IV) 폐암 환자들이 시작부터 글로벌 가이드라인에서 표준 치료로 권고하고 있는 키트루다의 치료 혜택을 부담 없이 받을 수 있게 됐다는 점에서 의미가 있다”며 “키트루다가 ▲임상 연구뿐만 아니라 ▲장기 추적 연구 결과와 ▲실제 진료환경 내 연구를 통해서 지속적으로 강력한 생존율 개선 및 반응률 혜택이 입증된 만큼, 키트루다 1차 치료로 국내 폐암 환자분들도 두 배의 내일을 만들어갈 수 있을 것으로 기대한다”고 말했다.
키트루다, 국내 진행성∙재발성 호지킨림프종 환자들의 생존율과 삶의 질 향상에 더욱 기여할 것
호지킨림프종 환자를 대상으로 진행된 KEYNOTE-204 연구 결과, 키트루다는 기존의 표준 치료였던 브렌툭시맙 베도틴 대비 불응성 또는 재발성 전형적 호지킨림프종 환자의 질병 진행 또는 사망 위험을 35% 감소시켰으며, 유의한 무진행 생존 기간 개선 효과(13.2개월 vs 8.3개월) 역시 확인했다. 또 반응이 있는 환자는 약 2년 동안 치료 효과가 유지됐고, 사회적 신체적으로 삶의 질 또한 향상됐다.
한국MSD 의학부 김수정 전무는 “호지킨림프종은 혈액암 중 가장 흔한 암인 악성림프종의 한 종류로, 젊은 층에서도 흔히 발생해 사회적 비용 부담이 큰 암이다. 특히 전형적 호지킨림프종에서 자가조혈모세포이식이 불가능하거나, 자가조혈모세포이식 이후 재발 또는 진행된 환자에서 보다 개선된 치료 옵션에 대한 미충족 의학적 수요가 상당했는데, 이번 급여 확대로 이 경우의 환자분들도 키트루다 치료를 통해 더 향상된 생존율과 삶의 질을 기대할 수 있게 되었다”라고 말했다.
한국MSD, 국내 암 환자들에게 더 나은 암 치료 혜택 제공 위한 연구와 투자 지속
김수정 전무는 이번 급여 확대 의미와 더불어, 키트루다의 한국 사회 기여 현황 및 국내 암 환자에게 더 건강한 내일을 선사하기 위한 한국MSD의 미션에 대해서도 발표했다.
MSD 주도로 진행 중인 글로벌 항암제 관련 연구 중 약 120건이 한국에서 진행되고 있다. 현재까지 국내 총 임상 참여 환자는 약 4,000명이며 전세계적으로 항암제 임상 시험에 가장 많이 참여하는 상위 10개 연구기관 중 4개가 한국에 위치해 있다.
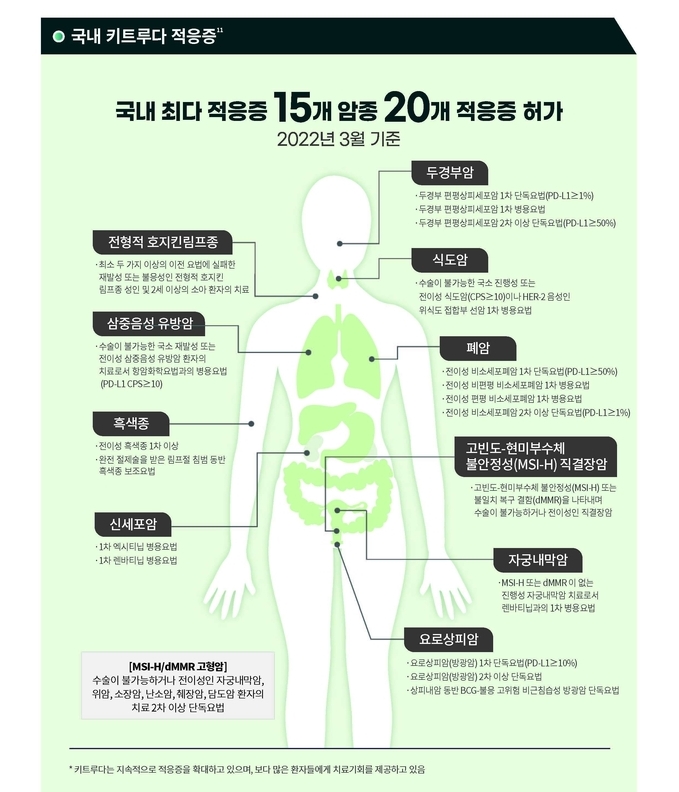
김수정 전무는 “키트루다는 항암 치료의 패러다임을 바꾼 치료 옵션으로, 국내 항암제 중 최다 적응증을 허가 받았으며 이번 급여 확대로 폐암, 호지킨림프종, 흑색종 등 총 3개 암종, 6개 적응증에 보험 급여가 적용된다. 한국MSD는 앞으로도 암 환자들의 수명 연장을 위한 임상 연구를 활발히 펼치며 키트루다가 가진 더 많은 가능성의 발견을 위해 노력할 것”이라고 소개했다.
한국MSD 케빈 피터스 대표는 “이제 더 많은 국내 환자분들께 키트루다를 통한 생존 연장의 기회와 삶의 질 향상 경험을 제공할 수 있게 되었다”며 “한국MSD는 항암 분야를 선도하는 회사로서, 앞으로도 더 많은 환자들이 키트루다를 비롯한 혁신적인 치료제의 혜택을 누릴 수 있는 환경을 만들기 위해 의료진, 연구자, 정부 등과 협력하며 최선을 다할 것”이라고 말했다.
*비소세포폐암 1차 병용, 비소세포폐암 1차 단독, 호지킨림프종 2차 이상 또는 3차 이상 단독, 비소세포폐암 2차 이상 단독, 흑색종 1차 이상 단독
**KEYNOTE-407: 크로스오버 조정값
***의료기관/연구자 중복 카운팅: 여러 연구에 참여하고 있는 의료기관이 대부분이어서, 중복집계됨 (2022년 3월 4일
MSD에 대하여
MSD는 130년 동안 ‘생명을 구하고 삶을 개선한다’는 사명을 추구하며, 전 세계 사람들의 삶에 의미 있는 변화를 만들기 위해 혁신 의약품, 백신을 개발해왔다. MSD는 의료접근성 향상을 통한 환자와 인류의 건강을 위해 전 세계 보건의료 전문가, 관련 기관 등과 협업하고 있다. 현재 암, HIV 및 에볼라를 포함한 감염질환, 새로운 동물질환 등 사람과 동물의 생명을 위협하는 질환의 예방과 치료를 위해 최선을 다하고 있다. 자세한 사항은 www.msd.com, 트위터, 링크드인, 유튜브에서 확인할 수 있다.
한국MSD에 대하여
한국MSD는 세계적인 바이오헬스케어 기업 MSD(Merck Sharp & Dohme Corp)의 한국법인이다. 1994년 설립 이래 100개 이상의 혁신적인 의약품백신 및 수준 높은 의학정보를 제공하며 한국인의 질병치료와 건강증진을 위해 노력해왔다. 한국MSD는 ‘삶을 위한 발명’이라는 기업철학의 국내 실현을 책임으로 여기며 한국인의 더 건강한 내일을 위해 전문가, 파트너사, 정부 당국 등과 함께 계속해서 노력할 것이다. 자세한 정보는 한국MSD 홈페이지(www.msd-korea.com) 및 페이스북에서 확인할 수 있다.
References
1 건강보험심사평가원 요양급여의 적용기준 및 방법에 관한 세부사항 공고. 2022-38호
2 통계청. 2020년 사망원인통계 결과 보도자료.
3 NCCN Guideline NSCLC (2022 V1)
4 D. Rodriguez-Abreu et al. Pemetrexed plus platinum with or without pembrolizumab in patients with previously untreated metastatic nonsquamous NSCLC: protocol-specified final analysis from KEYNOTE-189. Annals of Oncology Vol 32. 2021
5 Luis Paz-Ares et al. A randomized, placebo-controlled trial of pembrolizumab plus chemotherapy in patients with metastatic squamous NSCLC: protocol-specified final analysis of KEYNOTE-407. Journal of Thoracic Oncology Vol.15. 2020
6 Martin Reck et al. Five-Year Outcomes With Pembrolizumab Versus Chemotherapy for Metastatic Non-Small-Cell-Lung-Cancer With PD-L1 Tumor Proportion Score≥50%. Journal of Clinical Oncology. Vol 39. 2021
7 Julie R Brahmer, et al. Health-related quality-of-life results for pembrolizumab versus chemotherapy in advanced, PD-L1-positive NSCLC (KEYNOTE-024): a multicentre, international, randomised, open-label phase 3 trial. Lancet Oncol 2017.
8 John Kuruvilla et al. Pembrolizumab versus brentuximab vedotin in relapsed or refractory classical Hodgkin lymphoma (KEYNOTE-204): an interim analysis of a multicentre, randomised, open-label, phase 3 study. Lancet Oncol 2021; 22:512-24
10 Zinzani PL, Ramchandren R, Santoro A, et al. Quality-of-life analysis of pembrolizumab vs brentuximab vedotin for relapsed/refractory classical Hodgkin lymphoma. Blood Adv. 2022;6(2):590-599. doi:10.1182/bloodadvances.2021004970
11 대한혈액학회에서 제공하는 2017년 의학정보 ‘림프종’. 대한혈액학회지. 2017 August VOL.258
12 대한혈액학회. 환우와 가족을 위한 혈액 질환 소개서. 악성 림프종
13 Aldin A et al. Interim PET-results for prognosis in adults with Hodgkin lymphoma: a systematic review and meta-analysis of prognostic factor studies (Review). Cochrane Database of Systematic Reviews 2020, Issue 1. Art. No.: CD012643.