사노피-아벤티스 코리아(대표 배경은, 이하 사노피)가 9월 16일 ‘국내 아토피피부염 환자 대상 첫 실제 임상경험 결과 발표’를 주제로 미디어 세미나를 개최하였다.
온라인 라이브 스트리밍으로 진행된 이날 세미나에서는 국립중앙의료원 피부과 안지영 교수가 연자로 참석하였다.
안지영 교수는 국내 성인 중등도-중증 아토피피부염 환자를 대상으로 한 실제 임상경험을 비롯해 듀피젠트의 임상적 가치 및 아토피피부염 질환 정보에 대해 설명하였다.
다음은 이날 세미나 내용의 정리분이다.
Part 1. 아토피피부염에서의 듀피젠트® 국내도입 현황
1. 듀피젠트®의 국내 도입 현황 및 적응증
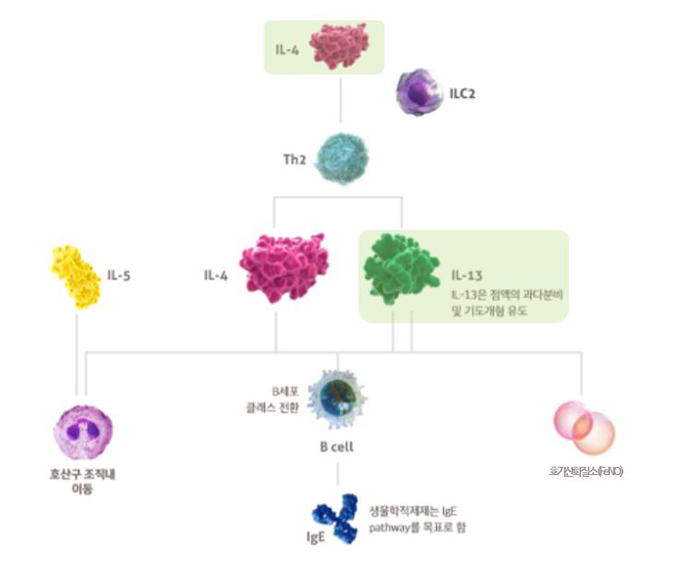
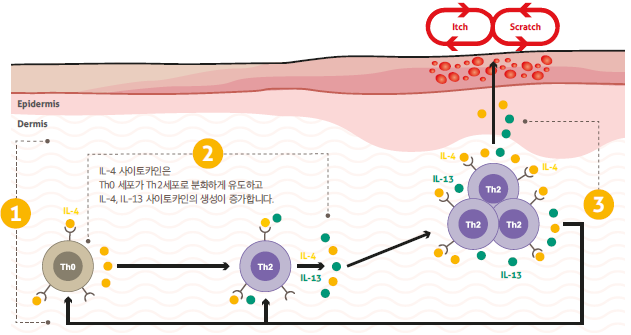
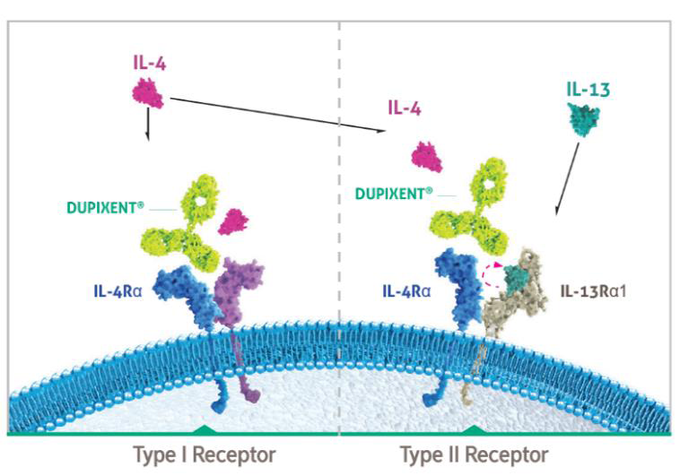
• 듀피젠트®프리필드주(성분명: 두필루맙, 유전자재조합)는 기존 국소요법으로 질환이 충분하게 조절되지 않거나 이러한 요법이 권장되지 않는 중등도–중증아토피피부염 환자를 위한 치료제로, 인터루킨(IL-4)와 인터루킨(IL-13) 사이토카인을 표적하는 아토피피부염 최초의 표적생물의약품(2020년9월기준)이다.
• 국내에는 2018년 3월 식품의약품안전처로부터 시판 허가를 받아 그 해 8월 출시되었다.2 이후 보건복지부고시에 따라 2020년 1월 1일부터 중증 성인아토피 피부염에 대하여 건강보험약제급여목록에 등재됐다.
• 2020년 4월 듀피젠트®는 만 12세 이상 청소년 중등도-중증 아토피피부염 환자에서의 사용 또한 승인된 바 있다. 이에 듀피젠트는 국소치료제로 적절히 조절되지 않거나 이들 치료제가 권장되지 않는 중등도에서 중증 12세 이상 청소년 및 성인 아토피피부염 환자의 치료 요법으로 적응증을 획득했다.5,6
2. 듀피젠트®의 국내급여기준
• 듀피젠트®는 몇 가지 조건에 준하여 아토피관련 진료과 (피부과, 알레르기내과, 소아청소년과(소아알레르기호흡기)) 전문의에 의해 처방될 때 급여 혜택을 받을 수 있다.4
• 급여 기준은 다음과 같다. 3년 이상의 병력을 가진 만18세 이상 성인 만성 중증 아토피피부염 환자로서 ▲듀피젠트® 투여시작 전 습진중증도평가지수(EASI)가 23 이상인 경우 ▲1차 치료제로 국소치료제(중등도 이상의 코리티코스테로이드 또는 칼시뉴린저해제)를 4주 이상 투여하였음에도 적절히 조절되지 않고, 이후 전신 면역억제제(사이클로스포린 또는 메토트렉세이트)를 3개월 이상 투여했음에도 EASI 50% 이상 감소 등 반응이 없거나 부작용 등으로 사용할 수 없는 경우 보험 급여가 인정된다.4
• 보험 급여 혜택을 지속적으로 받기 위해선, 14주 투여 후 16주차에 EASI가 75%이상 감소한 것으로 평가되어야 6개월 추가 투여가 인정된다. 이후 6개월마다 재평가를 통해 최초 평가 결과가 유지되는 것으로 확인될 경우 계속해서 보험 급여 혜택을 받을 수 있다.4
Part 2. 듀피젠트® 국내 실제 임상경험(Korea Real World Evidence)
1. 연구명 : 국내중등도-중증 아토피피부염 환자대상 국내 실제 투여경험을 바탕으로 한 듀피젠트®의 효과와 안전성 프로파일에 대한 후향적연구
2. 연구 개요
• 기간 : 2018년 9월부터 2019년 6월까지의 기간 동안 듀피젠트®로 치료받은 환자의 진료기록 후향적 분석7
• 대상 : 국내중등도-중증 아토피피부염환자 101명 (Age >18 years, EASI score >16)7
• 치료 방법 : 첫회 듀피젠트® 600 mg 투여, 이후 2주 또는 그 이상의 간격으로 300 mg 투여
* 환자에 따라 필요시 전신요법 병용7
3. 주요 연구 내용
• 국내 환자에서의 듀피젠트®의 치료효과와 안전성 프로파일을 확인하기 위해 진행된 이번 후향적 연구에서는 18세 이상 중등도-중증 아토피피부염 환자총 101명의 진료기록을 분석했다. 이들은 16주간 듀피젠트를 통해 치료받았다.7
• 듀피젠트® 투여군은 투여 2주차부터 습진중증도평가지수(EASI)와 숫자통증등급(NRS) 점수 개선이 관찰되었으며, 투여 16주차에 EASI 점수가 베이스라인(29점) 대비 77.4%가 개선되는 것을 확인했다.1 NRS 점수 또한 투여 16주차에 베이스라인(8점) 대비 70%가 개선되었다.7
• 특히 분석한 환자 중 63.6%가 투여 16주차에 베이스라인 대비 EASI-75 도달에 성공해,기존 글로벌 임상인 SOLO1(51%) 및 CHRONOS (69%) 연구와 비교하여도 유사한 효과를 입증했다.7,9
• 환자중심습진평가(POEM) 점수 또한 듀피젠트 투여 16주차에 베이스라인(24점) 대비 60.7% 개선되었으며, 피부삶의질점수(DLQI) 점수는 베이스라인(23점) 대비65%가 개선되었다.7
• 듀피젠트®를 투여받은 환자들은 높은 중증도와 기존 치료이력을 대부분 가지고 있었으며, 주요 이상반응은 안면의 홍반(9.9%)과 결막염(5%)이었다.7 이는 기존 글로벌 3상연구에서 나타난 이상반응과 유사하다.7
• 듀피젠트®는 국내 환자에서도 EASI, NRS, POEM, DLQI 등 아토피피부염 중증도를 평가하는 모든 평가 항목에서 유의한 개선을 보였다.7 이는 기존 글로벌 임상인 CHRONOS 및 SOLO 등 3상 연구에서 나타난 결과와 유사한 값으로, 듀피젠트®가 국내 환자에서도 특별한 이상반응 없이 치료효과를 입증한 것으로 해석할 수 있다.7
References
7 Jang DH, et al. J Clin Med 2020;9(6): DOI:10.3390/jcm9061982
8 Blauvelt A, et al. Lancet. 2017;389(10086):2287-2303
9 Simpson EL, et al. N Engl J Med. 2016;375:2335-2348.