신장 이식 환자 표준 치료 옵션으로의 가능성 제시
• 써티칸, 신장 이식 환자 대상으로 진행된 최대 규모 중개 연구인TRANSFORM 임상 분석 결과 전체 신장 이식 환자 대비 아시아 환자에서 높은 면역 억제, 신기능 보존 및 바이러스 감염 감소 효과 확인1, 2
• 한국인 가장 많이 포함된 TRANSFORM 아시아 지역 24개월 데이터 분석 결과, 써티칸 치료군이 마이코페놀산 치료군 대비 우월한 효과 보여1, 3
• 써티칸, TRANSFORM 아시아 데이터 통해 신장 이식 환자의 표준 치료 가능성 확인. 국내 신장 이식 환자들의 치료 접근성 향상 필요성 대두
노바티스가 자사의 이식면역억제제 써티칸®(성분명 에베로리무스)이 전체 신장 이식 환자에 비해 아시아 신장 이식 환자에서 더 우수한 치료 효과를 보인다는 TRANSFORM 연구 결과를 발표했다. 1 해당 결과는 11월 8일부터 10일까지 부산 벡스코에서 열린 대한이식학회 추계 학술대회(Asian Transplantation Week 2018)에서 발표됐다.
TRANSFORM 연구는 전세계 42개국 186개의 기관에서 모집된 2037명의 신장 이식 환자를 대상으로 실시한 최대 규모의 중재 연구로, 농도 조절된 써티칸과 노출 감소된 칼시뉴린 억제제(Calcineurin inhibitor, CNI) 병용요법을 마이코페놀산과 노출 표준의 CNI 병용요법과 비교 평가한 연구다. 2 아시아 지역 하위 분석 결과는 한국, 일본, 인도 등 8개국 총 262명 환자를 대상으로 하고 있으며, 이 중 한국 환자는 53명으로 가장 많았다. 1, 3
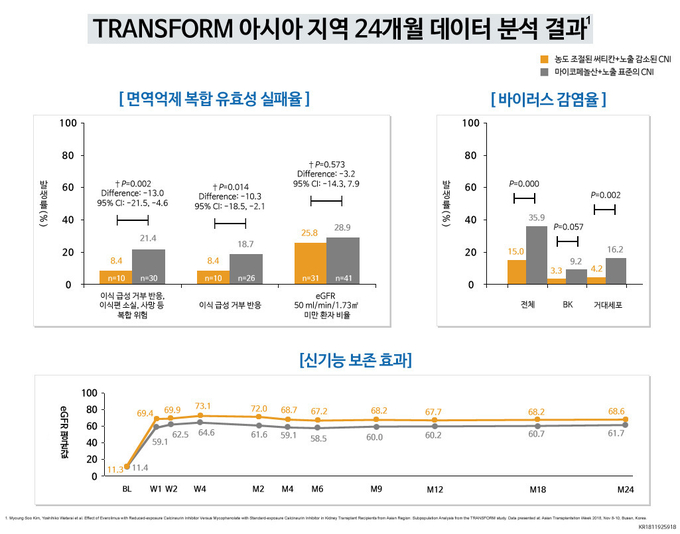
TRANSFORM 연구 아시아 지역 24개월 데이터 분석 결과, 써티칸 치료군의 치료된 생검-입증 급성 거부 반응 (tBPAR) 또는 MDRD4 공식에 의한 추정 사구체 여과율(eGFR)* 수치가 50 ml/min/1.73m2 미만인 환자 비율 (1차 유효성 평가 변수)은 26.7%로 대조군인 마이코페놀산 치료군의 38.0% 대비 낮은 경향을 보였다. (95% CI: -22.3, 0.5; P=0.061) 1, * 또 써티칸 치료군의 이식 급성 거부 반응, 이식편 소실, 사망 등 복합 위험은 8.4%로, 대조군의 21.4%에 비해 약 13%로 유의하게 낮췄다. (95% CI: -21.5, -4.6; P=0.002) 1 해당 결과를 통해 써티칸 군에서 대조군 대비 우월한 면역 억제 효과를 확인했다.
*추정 사구체 여과율(eGFR): 신장 기능을 평가하는 지표. 체표면적을 기준으로 사구체가 1분 동안 몇 mL를 여과할 수 있는지를 나타냄 4
이번 연구를 통해 써티칸의 유의한 신기능 보존 효과도 확인했다. 1 CNI는 신장 이식 환자에게 사용되는 표준 면역억제제이지만, 신독성을 유발하고 장기 노출 시 심혈관계 동반질환이나 악성종양을 유발할 수 있다. 5, 6, 7 이번 연구에서 마이코페놀산과 CNI 병용요법 대비 써티칸과 CNI 병용 시 모든 시간대에서 추정 사구체 여과율이 높게 유지됐다. 1
바이러스 감염율 역시 써티칸 치료군이 유의하게 낮았다. 1 이식 환자들은 이식 후 면역력이 저하돼 바이러스에 쉽게 감염될 수 있다. 8 감염 시 이식편의 소실 및 사망 위험이 높아져 바이러스 감염은 이식 후 평가에 중요한 지표다. 연구 결과, 각 치료군의 전체 바이러스 감염율은 각각 15.0%, 35.9%였으며, (P=0.000) 1 BK 바이러스(3.3% vs 9.2%, P=0.057) 감염율은 써티칸 치료군이 대조군 대비 약 3배 낮은 경향을 보였으며, 거대세포바이러스(4.2% vs 16.2%, P=0.002) 감염율은 써티칸 치료군이 대조군 대비 약 4배 낮았다. 1
이번 연구에 참여한 신촌 세브란스 병원 이식외과 김명수 교수는 “이번 TRANSFORM 연구 아시아 테이터 결과 통해 써티칸의 강력한 면역 억제 효과 및 신기능 보존 효과, 바이러스 감염 감소 효과까지 확인할 수 있었다. 특히 아시아 신장 이식 환자에서 탁월한 결과를 보여 써티칸의 신장 이식 환자의 표준 치료제로서 가능성을 확인했다”며 “신장 이식은 환자의 생명과 직결되어 있으며, 신장 이식 후 합병증, 바이러스 감염 등은 이식신의 기능과 밀접한 관련이 있는 문제인 만큼, 국내 신장 이식 환자들이 써티칸을 통해 장기 이식 거부 반응을 예방할 수 있도록 급여 적용 등 치료 접근성 향상이 고려될 필요가 있다”고 덧붙였다.
한편, 써티칸은 장기 이식 수술을 할 때 일어날 수 있는 거부반응을 예방하는 증식신호 억제제 계열의 mTOR 억제제로 경도, 중등도의 면역학적 위험을 가진 신장 및 심장 이식 및 간 이식을 받은 환자의 이식 후 장기 이식 거부 반응을 예방하는 치료제로 허가 받았으며, mTOR 억제제 중 심장∙신장 및 간 이식 모두에 적응증을 가진 유일한 약물이다. 9, 10
* TRANSFORM에 대하여2
TRANSFORM은 24개월, 오픈라벨, two-arm, 무작위 대조 4상 임상연구로, 42개국 186개의 기관에서 모집된 2,037명의 신장 이식 환자를 대상으로 실시한 최대 규모의 신생 병변 중재 연구다. TRANSFORM 연구에서는 농도 조절된 써티칸과 노출 감소된 칼시뉴린 억제제(Calcineurin inhibitor, CNI) 병용요법을 마이코페놀산과 노출 표준의 칼시뉴린 억제제 병용요법과 비교 평가했다.
연구에 참여한 환자들은 이식 후 24시간 이내에 1:1 비율로 무작위로 추출됐으며, 이는 기증자의 유형, 칼시뉴린 억제제 유형 등을 기반으로 계층화됐다. 1차 분석 결과는 12개월 후 이뤄졌다. TRANSFORM 연구의 1차 유효성 평가 변수는 이식 급성 거부 반응 발생률과 추정 사구체 여과율(eGFR)로 평가 이식편 기능이 50 ml/min 미만인 환자 비율이었으며, 2차 유효성 평가 변수에는 이식 급성 거부 반응, 이식편 소실, 사망 등이 포함됐다.
* 써티칸(Certican)에 대하여
써티칸은 장기 이식 수술을 할 때 일어날 수 있는 거부반응을 예방하는 증식신호 억제제 계열의 mTOR 억제제로 경도, 중등도의 면역학적 위험을 가진 신장 및 심장 이식 및 간 이식을 받은 환자의 이식 후 장기 이식 거부 반응을 예방하는 치료제로 허가 받았다. 9
써티칸(효능 효과) 신장 및 심장 이식: 경도, 중등도의 면역학적 위험을 가진 동종 신장 또는 심장 이식을 받은 성인 환자에서 이식 후 장기 이식 거부 반응의 예방. 신장 및 심장 이식에서 사용 시 이 약은 마이크로에멀젼 제형의 사이클로스포린 및 코르티코스테로이드와 병용하여 투여한다.
간이식: 간 이식을 받은 성인 환자에서 이식 후 장기 이식 거부 반응의 예방. 간 이식에서 사용 시, 이 약은 타크로리무스 및 코르티코스테로이드와 병용해서 투여한다. 9
* 노바티스(Novartis)에 대하여
노바티스는 인류의 생명 연장과 삶의 질 개선을 목표로 의약품 혁신에 매진하는 세계적인 제약 기업이다. 업계를 선도하는 노바티스는 최첨단 과학기술과 디지털 기술을 접목하여 사회와 환자가 필요로 하는 혁신적인 의약품 개발에 앞장서고 있으며, 매년 세계에서 R&D에 가장 많은 투자를 하는 기업 순위에 이름을 올리고 있다. 노바티스의 의약품으로 치료 받는 인구는 전 세계적으로 약 10억여명에 달하며 최신 의약품에 대한 환자 접근성을 높이는 혁신적인 방안들을 도입하고자 하는 노바티스의 노력은 현재도 계속되고 있다. 전 세계 각지에서 140여개 국가 출신 125,000명의 노바티스 임직원들이 근무하고 있다. 보다 자세한 내용은
http://www.novartis.com 확인할 수 있다.
* 한국노바티스(Novartis Korea)에 대하여
세계적인 제약•바이오 기업, 노바티스의 자회사인 한국노바티스(www.novartis.co.kr) 는 제네릭사업부인 한국산도스와 안과사업부인 한국알콘을 포함해 약 740 여 명의 직원을 두고 있다. 한국노바티스는 지난 10년 간 한국에서만 약 200 여 건의 임상시험을 진행하여 국내 연구진과의 협력을 활발히 진행하고 있으며, 환우 및 가족 정서 지원 프로그램인 ‘치유(CHEER YOU)’, 환우의 사회 복귀 지원 프로그램 ‘이음’, 여성 암환자 지원 프로그램인 ‘가화맘사성’과 매년 전 직원이 자원봉사활동에 참여하는 ‘지역 봉사의 날’ 행사 등 다채로운 사회공헌활동을 통해 지역 사회에 이바지하는 기업이 되기 위해 최선을 다하고 있다.
References
1. Myoung Soo Kim, Yoshihiko Watarai et al. Effect of Everolimus with Reduced-exposure Calcineurin Inhibitor Versus Mycophenolate with Standard-exposure Calcineurin Inhibitor in Kidney Transplant Recipients from Asian Region: Subpopulation Analysis from the TRANSFORM study. Data presented at: Asian Transplantation Week 2018, Nov 8-10; Busan, Korea.
2. Julio Pascual, Stefan Berger et al. Everolimus with Reduced Calcinuerin Inhibotor Exposure in Renal Transplantation. J Am Soc Nephrol 29: 1979-1999, 2018.
3. Julio Pascual, Stefan Chadban et al. Efficacy and Safety of Everolimus With Reduced-Dose Calcineurin Inhibitor in De Novo Kidney Transplant Recipients: Results from the TRANSFORM study. Data presented at: 27th International Congress of The Transplantation Society, June 30-July 5; Madrid, Spain.
4. 이나미, 임인석. 소아 환자에서 다양한 사구체 여과율 측정법의 비교. Korean Journal of Pediatrics. 2009, Vol 52. No 9.
5. J.R Chapman. Chronic Calcineurin Inhibitor Nephrotoxicity-Lest We Forget. American Journal of Transplantation 2011; 11: 693-697.
6. Allison Webber et al. Novel Strategies in Immonosuppression: Issues in Perspective. Transplantation. 2011, Vol 91. No 10.
7. Shelly Lichtenberg et al. The incidence of post-transplant cancer among kidney transplant recipients is associated with the level of tacrolimus exposure during the first year after transplantation. Eur J Clin Pharmacol (2017) 73:819-826.
9. 써티칸 제품설명서
10. 시롤리무스 효능효과