- 4가독감백신중 국내최초, 생후 6개월 이영유아에 접종허가[i]
- 온가족 접종가능한 4가독감백신으로 확대
- 영유아, 소아 및 청소년, 성인대상 임상연구결과 발표
GSK(한국법인 사장 줄리엔샘슨)는 6월 21일 4가독감백신 ‘플루아릭스테트라’의 생후 6개월 영유아 대상 출시를 기념하여 더플라자호텔에서 ‘One 4 ALL 기자간담회’를 열고 A·B형 독감바이러스를 예방하는 4가독감백신의 중요성 및 향후계획에 대해 발표했다.
GSK 플루아릭스테트라는 지난 4월 27일 국내에 소개된 4가독감백신중 최초로 식품의약품안전처로부터 생후 6개월 이상 3세 미만 소아를 대상으로 승인받았다.
이번에 접종연령대가 확대승인됨에 따라 생후 6개월 이상 영유아부터 소아 및 청소년, 성인 등 온가족이 접종가능한 4가독감백신1으로 도약하게 됐다.
이날 기자간담회에서 GSK 학술부 이재혁 부장은 독감의 질병부담과 국내외 역학을 소개하였다.
이어서 GSK 백신사업부 의학 및 공중보건 디렉터 필립부시 박사(Dr. Philippe Buchy, Director of Scientific Affairs and Public Health in GSK Vaccines)는 생후 6개월 이상 영유아부터 소아 및 청소년, 성인 임상 연구결과를 발표했다.
이번 생후 6개월 이상 영유아 승인의 근거가 된 임상연구결과에 따르면, 플루아릭스테트라는 2011년부터 2014년까지 5번의 독감시즌동안 13개국에서 생후 6개월~35개월 영유아 12,018명을 대상으로 실시한 연구결과, 독감감염으로 인한 보건의료 이용현황에 주요한 감소효과를 미쳤다.[ii],[iii]
영유아의 항생제 사용 50% 감소, 병·의원 방문 47% 감소, 부모의 회사결근 54% 감소, 응급실 방문 79% 감소가 관찰되었다.
중등도 내지 중증 독감에 대해 63.2% 예방효과를 보였고 전체 독감에 대해 49.8% 예방효과를 입증했다. 2
국소, 전신 이상반응에서는 대조군과 비교해 유사한 안전성 결과를 보였다.3
GSK 백신사업부 의학 및 공중보건 디렉터 필립부시 박사는 “이번 임상연구는 영유아를 대상으로 4가독감백신의 유효성을 평가하기 위해 실시된 최초의 임상연구다”라고 밝혔다.
필립부시 박사는 “한국에서 독감예방과 질병부담을 감소시키는데 중요한 역할을 할 플루아릭스테트라의 새로운 연구결과를 소개하게 되어 기쁘게 생각한다”고 말했다.
GSK 백신마케팅 정현주 팀장은 “생후 6~35개월 영유아는 감염위험이 높은 고위험군으로 최근 보육시설이나 단체생활로 인한 바이러스 노출과 지역사회로의 전파우려도 높다”며 “플루아릭스테트라의 접종연령 확대를 통해 영유아는 물론 전 연령층에 입증된 예방효과와 안전성을 기반으로 독감예방 혜택을 제공할 것으로 기대한다”고 말했다.
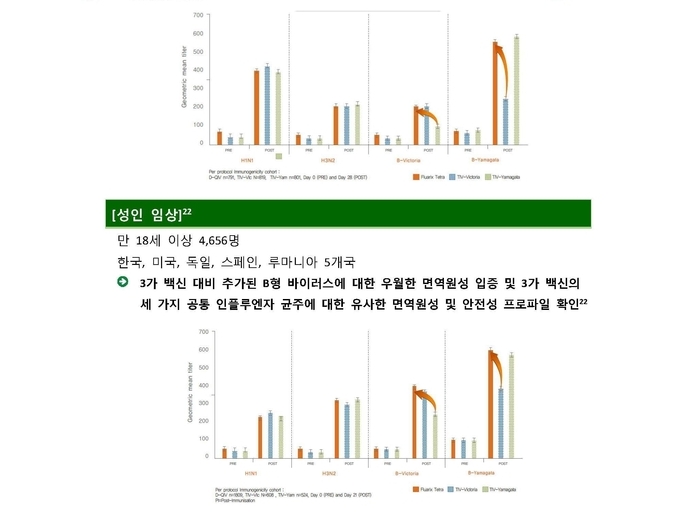
이밖에 이번 기자간담회에서는 플루아릭스테트라의 면역원성과 안전성 데이터를 확인하기 위해 소아 및 청소년, 성인대상으로 실시한 대규모 글로벌 임상연구 결과도 소개하여 각 연령그룹에 대한 플루아릭스테트라의 임상연구 결과들을 총망라한 자리가 되었다.
한편, GSK 플루아릭스테트라는 2016년에 이어 지난 해 2년 연속 4가독감백신부문 국내 판매 1위[iv]*(2017년 IQVIA Data 4Q 기준)를 달성하며 국내 1위 백신으로의 명성을 이어가고 있다.
국내[v]는 물론 세계 최초로 승인[vi],[vii],[viii],[ix],[x],[xi]된 불활화 4가독감백신 플루아릭스테트라는 전 세계 약 1억 7천만도즈 이상 공급[xii]돼 사용경험과 신뢰를 축적해 왔다.
독일 드레스덴13 생산설비의 엄격한 품질검사와 각 허가당국의 정기감사 등을 거쳐 생산[xiii],[xiv],[xv],[xvi], [xvii]되며, 미국, 영국, 호주의 국가예방접종사업(NIP) 백신에 선정되어 사용되고 있다.[xviii],[xix],[xx]
References
2 Carine Claeys et al. Prevention of vaccine-matched and mismatched influenza in children aged 6−35 months: a multinational randomized trial across five influenza seasons. The Lancet Child & Adolescent Health. Volume 2, Issue 5, May 2018, pages 338-349. Available at: http://dx.doi.org/10.1016/S2352-4642(18)30062-2 3 Claeys C, Zaman K, Dbaibo G, et al. Prevention of vaccine-matched and mismatched influenza in children aged 6−35 months: a multinational randomized trial across five influenza seasons. Lancet Child Adolescent Health 2018; published online March 5. http://dx.doi.org/10.1016/S2352-4642(18)30062-2 Supplementary appendix. 4 IQVIA data, Influenza Vaccine sales, 2017 4Q
7 US FDA, December 14, 2012 approval letter - Fluarix Quadrivalent
8 US FDA, June 7, 2013 approval letter - Fluzone Quadrivalent
9 US FDA, August 15, 2013 approval letter - FluLaval Quadrivalent
10 US FDA, May 23, 2016 approval letter - Flucelvax Quadrivalent
11 US FDA, August 26, 2016 approval letter - Afluria Quadrivalent
13 GSK data on file (GSK Biologicals Dresden your manufacturer for Fluarix Tetra)
22 질병관리본부예방접종별정보-인플루엔자:
http://www.cdc.go.kr/CDC/health/CdcKrHealth0101.jsp?menuIds=HOME001-MNU1132-MNU1147-MNU0746-MNU2422&fid=7955&cid=68890 (Last accessed April 2018)
*인용데이터: 2016년 2Q ~ 2017년 4Q IQVIA Sales Audit 참조. IQVIA데이터는 패널로부터 받은 유통자료를 통계처리한 추정치로써 실제와 다를 수 있으며, IQVI는 본 데이터의 활용으로부터 발생하는 분쟁에 대하여 여타의 책임을 지지 않음.