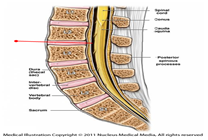
* 뉴로나타-알주(자가골수유래중간엽줄기세포)
* 제품 개요(희귀의약품)
ㅇ 제품명 : 뉴로나타-알 주(자가골수유래 중간엽줄기세포)
ㅇ 제조사 : 코아스템(주)
ㅇ 효능효과 : 리루졸과 병용하여 근위축성측삭경화증 환자에서 질환 진행속도 완화
| |
ㅇ 용법용량 : kg 당 1X106 세포를 요추뼈 2, 3번 사이 뇌척수강 내로 4주 간격으로 2회 투여
ㅇ 치료적 탐색 임상시험 : 시험군(33명, 리루졸과 뉴로나타-알주 병용)과 대조군(31명, 리루졸 단독)과의 4개월째 기능평가점수 변화량 비교
* 기능평가점수(ALSFRS-R) 변화량 : 시험군 -1.69, 대조군 –4.66
* ALSFRS-R(ALS functional rating scale-revised) : 신체적 기능(구기능, 소근육운동기능, 대근육운동기능, 호흡기능 등 4개 분류 12개 항목) 평가, 0(중증)~48(정상)
ㅇ 의의 : 적절한 치료방법이 적은 희귀질환인 루게릭병 환자에게 새로운 치료기회를 제공
* 루게릭병 환자 매년 10만 명당 1~2명 발생, 현재 국내 환자 약 2500명 내외 추정
* 참고사항
ㅇ 희귀의약품 지정(2013.12.31.)
ㅇ 해외 임상시험 진행
- 국제임상시험데이타베이스(www.clinicaltrials.gov)에 따르면 줄기세포를 이용한 루게릭병 환자 대상 임상시험은 미국 등에서 총 19건이 진행되고 있으며, 그 중 골수유래 중간엽줄기세포는 11건임.
* 총 19건 중 현재 임상 2상 진행 중인 것은 3건(미국2건, 인도1건)
* 희귀의약품 지정 및 허가
ㅇ 희귀의약품 지정제도
- 적용대상이 드물고 적절한 치료방법이나 의약품이 개발되지 않은 질환에 사용하는 의약품을 “희귀의약품”으로 지정하여 신속 허가 및 공급하는 제도임
* 희귀의약품의 경우 신속심사 대상, 허가신청수수료 50% 감면혜택
ㅇ 지정 요건(식약처 고시, ‘희귀의약품 지정에 관한 규정’)
- 국내 환자수(유병인구) 20,000명 이하인 질환에 사용되는 의약품
- 적절한 치료방법과 의약품이 개발되지 않는 질환에 사용하거나 기존 대체의약품보다 현저히 안전성 또는 유효성이 개선된 의약품
- 총 수입실적 150만불 이하, 총 생산실적 1 5억 이하인 의약품. 단, 환자수(유병인구)가 500명 이하인 경우 총 수입실적 500만불 이하, 총 생산실적 50억원 이하
ㅇ 희귀의약품 허가(식약처 고시, ‘생물학적제제 등의 품목허가·심사 규정’)
- 희귀의약품의 경우 동 의약품의 특성에 적합한 치료적 확증 임상시험자료를 제출하는 것을 조건으로 하여 탐색적 임상시험자료를 치료적 확증임상시험자료로 갈음할 수 있다.
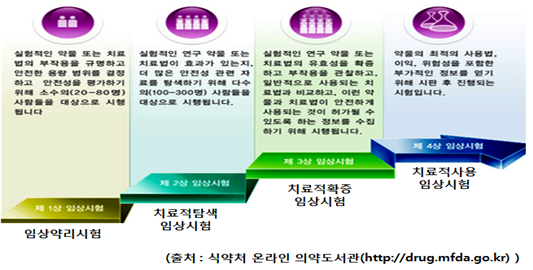
< 임상시험실시 단계에 따른 분류 >
* 줄기세포치료제 품목허가 현황(‘14.7월 현재)
1) 국내 허가 현황
업체수 | 품목수 | 세포기원 | 세포유래 | |||
자가 | 동종 | 골수 | 제대혈 | 지방 | ||
4 | 4 | 3 | 1 | 2 | 1 | 1 |
2) 국내 허가 품목 리스트
| 제품명 | 업체명 | 분류 | 대상질환 | 허가일자 |
1 | 하티셀그램- 에이엠아이 | 파미셀㈜ | 자가골수유래중간엽줄기세포 | 급성심근경색환자에서 좌심실구혈율 개선 | 2011.07.01 |
2 | 카티스템 | 메디포스트㈜ | 동종제대혈유래중간엽줄기세포 | 퇴행성 또는 반복적 외상으로 인한 골관절염 환자(ICRS grade IV)의 무릎 연골결손 치료 | 2012.1.18 |
3 | 큐피스템 | ㈜안트로젠 | 자가지방유래중간엽줄기세포 | 크론병으로 인한 누공 치료 | 2012.1.18 |
4 | 뉴로나타-알주 | 코아스템㈜ | 자가골수유래중간엽줄기세포 | 근위축성측삭경화증(루게릭병)환자에서 질환 진행속도 완화 | 2014.07.30 |
3) 해외 줄기세포치료제 허가 현황
국가명 | 제품명 | 업체명 | 분류 | 대상질환 | 허가일자 |
캐나다 | Prochymal | Osiris | 동종골수유래줄기세포치료제 | 이식편대숙주질환 | 2012.05.17 |